实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历下列过程,
已知Fe3+在pH=5时已完全沉淀,其中分析错误的是
| A.利用CuCO3替代CuO也可调节溶液的pH,不影响实验结果 |
| B.步骤②中发生的主要反应为:H2O2+2Fe2++2H+=2Fe3++2H2O |
| C.洗涤:向装晶体的漏斗中加水至浸没晶体,待自然流下后重复2~3次 |
| D.某实验需要240 mL1mol/L的CuSO4溶液,则配制时需称量CuSO4·5H2O 60g |
下列说法不正确的是()
| A.铅蓄电池在放电过程中,负极、正极质量都增加 |
B.常温下,反应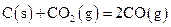 不能自发进行,则该反应的 不能自发进行,则该反应的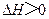 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
D.相同条件下,溶液中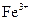 、 、 、 、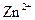 的氧化性依次减弱 的氧化性依次减弱 |
常温下,下列各组离子在指定溶液中能大量共存的是()
| A. |
的溶液中: 、 、 、 ; |
| B. |
由水电离的 的溶液中: 、 、 、 ; |
| C. |
的溶液中: 、 、 、 ; |
| D. |
D |
在100mL0.1mol/L 的醋酸溶液中,欲使醋酸的电离度增大,H+浓度减小,可采用的方法是()
| A.加热 | B.加入1mol/L 的醋酸溶液100mL |
| C.加入少量的0.5mol/L的硫酸 | D.加入少量的1mol/L 的NaOH溶液 |
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A.HCN是共价化合物 |
| B.HCN易溶于水 |
| C.10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 |
| D.c(H+)和溶液体积均相同的氢氰酸与盐酸相比,前者中和能力强 |
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③NaCl固体 ④CH3COONa固体 ⑤KCl溶液
| A.①② | B.②③⑤ | C.②④ | D.②④⑤ |