(10分) 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l )的燃烧热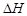 分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是 kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的
情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃) 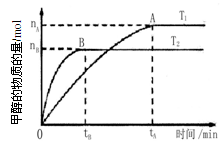
下列说法正确的是 (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为n(CH3OH)=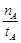 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时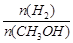 增大
增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为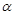 ,则容器内的压强与起始压强之比为 .
,则容器内的压强与起始压强之比为 .
某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。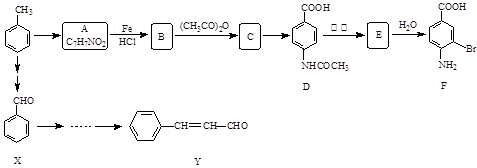
已知: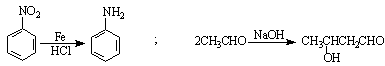
请回答下列问题:
(1)下列有关F的说法正确的是。
| A.分子式是C7H7NO2Br | B.能形成内盐 |
| C.能发生取代反应和缩聚反应 | D.1 mol的 F最多可以和2 mol NaOH反应 |
(2)C→ D的反应类型是 。
(3) B→C的化学方程式是 。在合成F的过程中,B→C步骤不能省略,理由是。
(4)D→E反应所需的试剂是 。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出3个)。
①苯环上只有两种不同化学环境的氢原子②分子中含有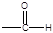
(6)以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图: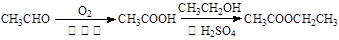
某些金属及金属氧化物对H2O2的分解反应具有催化作用,请回答下列问题: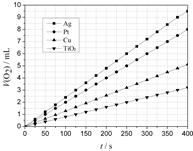
(1)已知:2H2O2(aq) =" 2" H2O (l) + O2(g) 的 < 0, 则该反应的逆反应能否自发进行?(填“能”或“不能”),判断依据是。
< 0, 则该反应的逆反应能否自发进行?(填“能”或“不能”),判断依据是。
(2)某同学选用Ag、Pt、Cu、TiO2作为催化剂,在25℃ 时,保持其它实验条件相同,测得生成的O2体积(V)。V与分解时间(t)的关系如图所示(O2的体积已折算成标准状况),则:在不同催化剂存在下,H2O2分解反应的活化能大小顺序是 Ea( ) > Ea( ) > Ea( ) > Ea( ) (括号内填写催化剂的化学式)金属Pt 催化下,H2O2分解的反应速率v(O2) =mol·s-1
(3)为研究温度对H2O2分解速率的影响(不加催化剂),可将一定浓度和体积的H2O2置于密闭容器中,在某温度下,经过一定的时间t,测定生成O2的体积V。然后保持其它初始条件不变,改变温度T,重复上述实验。获得V(O2) ~ T关系曲线。下列趋势图最可能符合实测V(O2) ~ T关系曲线的是,原因是。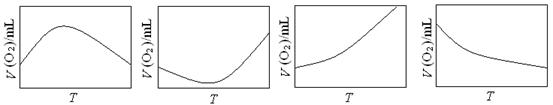
| A. | B. | C. | D. (4)以Pt为电极电解H2O2也可产生氧气,写出H2O2水溶液电解过程中的电极反应式(已知:H2O2的氧化性及还原性均比H2O强):阴极;阳极 。 |
某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)该研究小组是否成功制得 +1价Ca的化合物?(填“是”或“否”)。甲的化学式是。
(2)甲与水反应可得H2,其化学方程式是。反应所得溶液经结晶后,可得到一种晶体,其化学式为CaCl2· xCa(OH)2· 12H2O。为确定x的值,请设计实验方案。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料)。
芳香化合物A(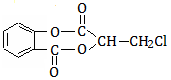 )在一定条件下可以发生如下图所示的转化(其他产物和水已略去)。
)在一定条件下可以发生如下图所示的转化(其他产物和水已略去)。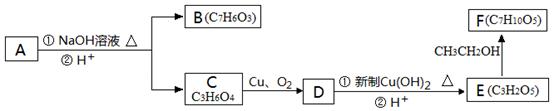
请回答下列问题:
(1)请写出A的分子式。
(2)1molA在氢氧化钠溶液中加热,充分反应消耗氢氧化钠mol。
(3)有机物C可以由乳酸(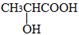 )经过几步有机反应制得,其中最佳的次序是:。
)经过几步有机反应制得,其中最佳的次序是:。
a.消去、加成、水解、酸化 b.氧化、加成、水解、酸化
c.取代、水解、氧化、酸化 d.消去、加成、水解、氧化
(4)写出由E制得F的化学方程式:,反应类型是。
(5)有机物B与乙酸酐(CH3COOCOCH3)直接反应制得阿司匹林(即乙酰水杨酸,分子式C9H8O4),满足以下条件的阿司匹林的同分异构体有种,写出其中任意两种的结构简式:、
。
①苯环上只含有两个侧链②有两个酯基③能发生银镜反应
已知A、B、C、D、E、F六种短周期元素的性质或结构信息如下表,请根据信息回答下列问题。
| 元素 |
性质或结构信息 |
| A |
单质常温下为固体,难溶于水易于溶CS2。能形成2种二元含氧酸。 |
| B |
原子的M层有1个未成对的p电子。核外p电子总数大于7。 |
| C |
单质曾被称为“银色的金子”。与锂形成的合金常用于航天飞行器。单质能溶强酸和强碱。 |
| D |
原子核外电子层上s电子总数比p电子总数少2个。单质和氧化物均为空间网状晶体,具有很高的熔、沸点。 |
| E |
其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高。 |
| F |
周期表中电负性最大的元素 |
(1)A原子的最外层电子排布式 ,D原子共有 种不同运动状态的电子。
(2)F与E元素第一电离能的大小关系: > (填元素符号)。
(3)A,B两元素的氢化物分子中键能较小的是 ;分子较稳定的是 。(填分子式)
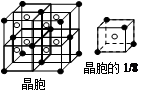
(4)C单质、镁、NaOH溶液可以构成原电池,则负极的电极反应式为_________________。
(5)F与钙可组成离子化合物,其晶胞结构如图所示,该化合物的电子式是 。已知该化合物晶胞1/8的体积为2.0×10-23cm3,求该离子化合物的密度,请列式并计算(结果保留一位小数):_______________________。