为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸的浓度和体积;②碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的物质的量;⑥反应前后的温度变化;⑦操作所需时间;
| A.①②③⑥⑦ | B.①③④⑤ | C.③④⑤⑥ | D.①②③④⑤⑥ |
下面的能源中属于二次能源的是
| A.电能、蒸汽 | B.电能、风能 |
| C.蒸汽、风能 | D.煤、石油 |
已知元素的原子序数,可以推知原子的①中子数 ②核电荷数 ③核外电子数 ④在周期表中的位置,其中正确的是
| A.①③ | B.②③ | C.①②③ | D.②③④ |
在加热固体NH4Al(SO4)2·12H2O时,固体质量随温度的变化曲线如图所示:已知A点物质为NH4Al(SO4)2 ,B点物质为Al2 (SO4) 3 ,下列判断正确的是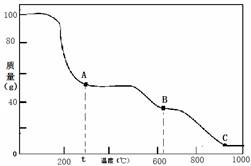
| A.0℃→t℃的过程变化是物理变化 |
| B.C点物质是工业上冶炼铝的原料 |
| C.A→B反应中生成物只有Al2 (SO4) 3和NH3两种 |
D.Al2 (SO4)3能够净水,可用离子方程式表示为:Al3++3OH- Al(OH)3 Al(OH)3 |
锂离子电池种类很多,其中有一种锂电池,用金属锂和石墨做电极材料,电解质溶液时由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)而形成的,电池总反应为8Li+3SOCl2=6LiCl+Li 2SO3 +2S则下列叙述中错误的
| A.电解质溶液中混入水,会影响电池反应 |
| B.反应中亚硫酰氯既是溶剂,又是氧化剂 |
| C.电池工作(放电)过程中,亚硫酰氯(SOCl2) 被还原为Li2 SO3 |
| D.电池工作过程中,金属锂提供的电子与正极生成的硫物质的量之比为4:1 |
室温下,下列溶液中粒子浓度关系正确的是
| A.KAl(SO4)2溶液:c(SO42-)>(K-)= c(Al3+ ) >c(H+)> c(OH-) |
| B.NaHCO3溶液:c(Na+)+c(H+)=c(CO32-)+c(OH-) + c(HCO3-) |
| C.Na2S溶液:c(OH-)-(H+)=c(HS-)+c(H2S) |
| D.CH3COONa与HCl混合后呈中性的溶液:c(Na+) > c(Cl-)= c(CH3COOH) |