盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。已知室温下:Ka(CH3COOH)=1.7×10-5 mol·L-1 ;H2CO3的电离常数Ka1=4.2×10-7mol·L-1 、 Ka2=5.6×10-11mol·L-1
(1)①请用离子方程式解释碳酸氢钠水溶液显碱性的原因 。
②常温下,物质的量浓度相同的下列四种溶液:
a、碳酸钠溶液 b、醋酸钠溶液 c、氢氧化钠溶液 d、氢氧化钡溶液
其PH由大到小的顺序是: (填序号)。
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是 ;该醋酸溶液稀释过程中,下列各量一定变小的是 。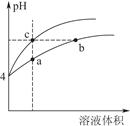
a.c(OH-) b.c(H+)
c.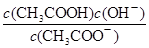 d.
d.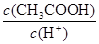
(3)以0.10 mol·L-1NaOH为标准液,测定某盐酸的浓度。取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
| 实验编号 |
氢氧化钠溶液的浓度 (mol·L-1) |
滴定完成时,氢氧化钠溶液滴入的体积(mL) |
待测盐酸的体积(mL) |
| 1 |
0.10 |
24.12 |
20.00 |
| 2 |
0.10 |
23. 88 |
20.00 |
| 3 |
0.10 |
24.00 |
20.00 |
①滴定达到终点的标志是___________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为__________________。
(4)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13,则:
①该温度下水的离子积常数Kw= mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH= 。
现有A、B、C、D四种化合物,透过蓝色钴玻璃其焰色反应均为紫色,A、B、C和盐酸发生反应后,均得到D;将固体C加热可得到A;若在A的溶液中通入一种无色无味气体,可制得C;若B与C的溶液混合可制得A。推断:
A为 ;B为 ;
C为 ;D为 。
写出有关反应的化学方程式:。
由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的某几种组成的混合物,加入盐酸放出的气体通过过量NaOH溶液后,气体体积有所减小。将上述混合物在空气中充分加热,有气体放出,且残留固体质量有所增加。由此可知混合物中一定含有_________,不能确定是否含有_______。
呼吸面具里有Na2O2,可吸收CO2放出O2,若用超氧化钾(KO2)代替过氧化钠,也能吸收CO2生成碳酸盐和O2。
(1)写出KO2与CO2反应的化学方程式。
(2)1 kg Na2O2和1 kg KO2与CO2反应生成O2的质量分别为__________。
(3)你认为选用_________作为氧化剂更为合适,理由是____________。
将一定量的纯碱溶于水,与适量盐酸反应。根据下列情况,填写盐酸和产生气体的量的变化。(1)若纯碱中含有K2CO3,盐酸用量将_______,产生气体的量将_______。
(2)若纯碱中含有NaHCO3,盐酸用量将_______,产生气体的量将_______。
(3)若纯碱中含有NaCl,盐酸用量将_______,产生气体的量将_______。
(4)若纯碱中含有NaOH,盐酸用量将_______,产生气体的量将_______。
A、B、C、D、E、F六种物质都易溶于水,水溶液除F外都能使石蕊试液变蓝色,六种物质的火焰都呈黄色。A、B与水反应时都有气体产生,A放出的气体有还原性,B放出的气体有氧化性,A、B溶于水都能生成C,C与适量CO2反应生成D。C与过量CO2反应生成E,而固体E加热可生成D。F的水溶液能使石蕊液变红,在F的溶液中加BaCl2溶液产生白色沉淀。F与D反应生成CO2,试判断
A________________ B________________,
C________________ D________________,
E________________ F________________。