下列说法正确的是
| A.硫酸、纯碱、硝酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B.根据元素种类的多少将物质分为纯净物和混合物 |
| C.通常情况下,若发生反应A2 + 2B-= 2A-+ B2,则氧化剂是A2 |
| D.碳酸氢钠在水中的电离方程式:NaHCO3=Na++H++CO32- |
下列叙述正确的是
| A.NH4Cl和CaC2都是离子化合物 |
| B.由碳氮原子形成的某种化合物比金刚石还坚硬,其主要原因是碳氮键比碳碳键更长 |
| C.因为液态氟化氢中存在氢健,所以其分子比氯化氢更稳定 |
| D.若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m+10 |
对下图两种化合物的结构或性质描述正确的是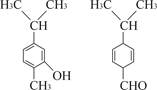
| A.不是同分异构体 |
| B.分子中共平面的碳原子数相同 |
| C.均能与溴水反应 |
| D.可用红外光谱区分,但不能用核磁共振氢谱区分 |
已知33As、35Br位于同一周期。下列关系正确的是
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
下列有关晶体的说法中一定正确的是
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
| A.①③ | B.只有⑤ | C.②④⑤ | D.③⑤ |
下列说法正确的是
①乙烯的结构简式:CH2CH2
②HF的电子式:
③HClO的结构式:H—O—Cl
④基态碳原子的价电子排布图:
⑤基态Cr的价电子排布式:3d44s2
⑥斜长石KAlSi3O8的氧化物形式可表示为:K2O•Al2O3•6SiO2
| A.①③ | B.③④ | C.④⑤ | D.③⑥ |