(10分)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________方法区别晶体、准晶体和非晶体。
(2)基态Fe原子有_______个未成对电子,Fe3+的电子排布式为_________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为____________。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道为___________,1mol乙醛分子中含有的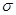 键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
(4)Al单质为面心立方晶体,晶胞中铝原子的配位数为 。
A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1 mol•L-1。反应进行2min后A的浓度为0.8 mol•L-1,B的浓度为0.6 mol•L-1,C的浓度为0.6 mol•L-1。则2min内反应的平均速率v(A)=____________,v(B)=_________________,v(C)=_______________。该反应的化学反应方程式为:______________________________。
由氢气和氧气反应生成1 mol水蒸气放热241.8 kJ,写出该反应的热化学方程式__________________________________。若1g水蒸气转化成液态水放热2.444 kJ,则反应2H2(g)+ O2(g) ===2H2O(l)的△H=_______________,氢气的燃烧热为_______________。
下列电解质中,①NaCl;②NaOH;③NH3·H2O;④CH3COOH;⑤BaSO4;⑥AgCl;⑦Na2O;⑧K2O;⑨H2O,________________是强电解质;______________是弱电解质
向100 ml浓硫酸中加入64 g铜片,加热一段时间后,至不再反应为止,请回答下列问题:
(1)写出反应的化学方程式:。
(2)若反应中有1.5 mol电子转移,被还原的硫酸为mol,标准状况下生成的SO2气体体积为L。
(3)将(2)反应后液体过滤,加水稀释滤液至500 ml,加足量Zn粉,经足够长的时间后,放出标准状况下6.72L H2,则反应的Zn的质量为g,原浓硫酸的物质的量浓度为mol·L-1。
某硫酸厂以硫铁矿为原料生产硫酸,主要过程的化学反应情况如下:
| 生产过程 |
化学反应 |
反应情况 |
| 硫铁矿的燃烧 |
4+11O2 2Fe2O3+8SO2 2Fe2O3+8SO2 |
4%的硫元素损失而混入炉渣 |
| SO2的接触氧化 |
2SO2+O2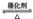 2SO3 2SO3 |
SO2转化率为95% |
| SO3的吸收 |
SO3+H2O=H2SO4 |
SO3的吸收率为98% |
(1)将硫铁矿燃烧的化学方程式补充完整:4+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)该厂现用100吨含硫40%的硫铁矿生产硫酸,可生产98%的浓H2SO4多少吨?(除上述硫的损失外,忽略其它损失)