可逆反应:X+Y W+Z,反应速率(V)随时间(t)变化的情况如图所示。
W+Z,反应速率(V)随时间(t)变化的情况如图所示。 表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
| A.t0时条件改变引起的变化是平衡向正反应方向移动 |
| B.若t0改变的条件是压强,则W、Z均为气体,X、Y中只有一种为气体 |
| C.若t0改变的条件是温度,则该反应的正反应是吸热反应 |
| D.若t0改变的条件是浓度,改变的方法是减小X、Y的浓度 |
下列关系正确的是
| A.含氢量:苯>乙烯>甲烷 |
| B.密度:H2O >溴苯 > |
| C.沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 |
| D.等质量的下列物质燃烧耗O2量:乙炔>乙烯>乙烷 |
下列有机物的命名中,正确的是
| A.3—甲基—1—丁烯 | B.2—乙基丁烷 |
| C.2,2—二甲基—4—丁醇 | D.2,3,3—三甲基丁烷 |
下列分子式表示的物质一定是纯净物的是
A.C2H6O B.C2H4Cl2 C.CH4O D.
设NA为阿伏加德罗常数,下列有关说法正确的是
| A.0.5 mol苯分子中含有C=C双键数为1.5 NA |
| B.1 mol甲基(—CH3)所含的电子总数为10 NA |
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为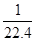 NA NA |
| D.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
有如下4种碳骨架的烃,其中表示碳原子,表示碳碳单键,未画出的键表示碳原子与氢原子相连,则下列说法正确的是


| A.a和c互为同分异构体 | B.b能使酸性高锰酸钾溶液褪色 |
| C.b和c互为同系物 | D.常温下d为气体 |