短周期元素X、Y、Z、W、Q在元素周期表中的位置如下表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是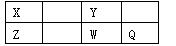
| A.W得电子能力比Q强 |
| B.由Z与Y组成的物质在熔融时能导电 |
| C.钠与Y可能形成Na2Y 2化合物且该化合物离子键和共价键 |
| D.X有多种同素异形体,而Y不存在同素异形体 |
某同学对“CO2是共价化合物和NH4Cl是离子化合物”,有下列四点感悟,其中不正确的是
| A.离子化合物中可能含共价键 |
| B.共价化合物中一定不含离子键 |
| C.离子化合物中不一定含金属元素 |
| D.离子化合物中一定不含共价键 |
已知:
下列说法不正确的是
| A.①和②变化过程中都会放出热量 |
| B.氯原子吸引电子的能力强于钠原子和氢原子 |
| C.①和②中的氯原子均得到1个电子达到8电子稳定结构 |
| D.NaCl中含有离子键,HCl中含有共价键 |
含有极性键的共价化合物是
| A.Na2O2 | B.NaOH | C.H2 | D.HC1 |
下列物质的电子式书写正确的是
A. |
B. |
C. |
D. |
下列物质中,只含有离子键的是
| A.NaOH | B.NH 4Cl | C.MgCl2 | D.H2O |