常温下,下列溶液的pH或微粒的物质的量浓度关系不正确的是
| A.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后混合后,溶液的pH=7,则反应后的混合后,2c(R2-)+c(HR-)="c(Na+)" |
| B.0.05mol/L的CH3COOH溶液中加入等体积的0.05mol/L的KOH溶液,则:c(CH3COOH)+c(H+)="c(OH-)" |
| C.pH=5的CH3COOH溶液和pH=5NH4Cl溶液中c(H+)相等 |
| D.0.2mol/L NH4Cl和0.1mol/L NaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
如图带漏斗U型管中装有足量的煤油和水的混合物,静置后投入一小块碱金属。可观察到金属在煤油和水的界面a附近上下往复运动,下列说法不正确的是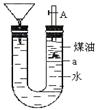
| A.此碱金属可能是钾或钠 |
| B.反应一段时间煤油会燃烧 |
| C.碱金属上下运动是由于与水反应产生了氢气 |
| D.若是金属锂则不能观察到上述现象 |
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X不可能是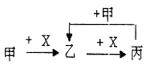
A.甲:Na、X:O2B.甲:NaOH溶液、X:CO2溶液
C.甲:C、X:O2D.甲:AlCl3溶液、X:NaOH溶液
以NA表示阿伏伽德罗常数,下列说法中正确的是
①58.5 g氯化钠固体中含有NA个氯化钠分子;
②5.6 g铁粉与酸反应失去的电子数一定为0.2 NA;
③6.0 g金刚石中含有的共价键数为NA;
④标况下,11.2 L SO3所含的分子数为0.5 NA;
⑤1L 1 mol·L-1 AlCl3溶液中含有NA个胶粒Al3+;
⑥常温下,42 g C2H4和C4H8的混合物中含有的碳原子数为3 NA
| A.⑤⑥ | B.④⑤⑥ | C.③⑥ | D.①②③ |
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
| A.铈(Ce)元素在自然界中主要以单质形式存在 |
| B.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI = CeI4 + 2H2↑ |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+ = Ce3++2Fe3+ |
D.四种稳定的核素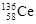 、 、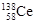 、 、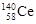 、 、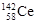 ,它们互称为同位素 ,它们互称为同位素 |
标况下有以下四种气体:①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S④0.2molNH3。下列对四种气体的关系从小到大表示不正确的是( )
| A.体积:④<①<③<② | B.质量: ④<①<③<② |
| C.物质的量:①<②<③<④ | D.氢原子数: ②<④<③<① |