(9分)某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置己略去,粗黑线表示乳胶管。请填写下列空白:

(1)甲装置常常浸在温度为70~80℃的水浴中,目的是 。
(2)实验时,先加热玻璃管乙中的镀银钢丝,约1分钟后鼓入空气,此时铜可丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
(3)乙醇的催化氧化反应是 反应(填“放热”或“吸热”),该反应的化学方程式为 。
(4)在实验过程中控制鼓气的速度很重要:
①控制鼓气速度的方法是 ,
②若鼓气速度过快反应会停止,原因: ,
③若鼓气速度过慢反应也会停止,原因: 。
(5)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、 接丙。
下列物质的转化或分离是用哪种方法实现的?
| A.溶解 | B.裂解 | C.分馏 | D.裂化 E.干馏 F.蒸馏 |
G.电解 H.过滤 I.萃取
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法)
(1)把煤转化为焦炉气、煤焦油和焦炭等
(2)从原油中分离出汽油、煤油、柴油等
(3)将海水淡化;(4)除去粗盐溶液中的泥沙
(5)从海水得到的无水MgCl2中提取金属镁
(6)海水提溴获得的溴水中,提取溴单质。
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下: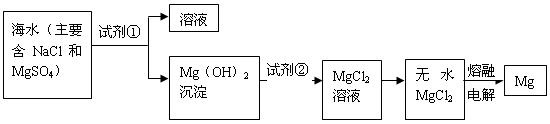
(1)为了使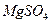 转化为
转化为 ,试剂①可以选用,要使
,试剂①可以选用,要使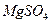 完全转化为沉淀,加入试剂①的量应;
完全转化为沉淀,加入试剂①的量应;
(2)加入试剂①后,能够分离得到 沉淀的方法是;
沉淀的方法是;
(3)试剂②可以选用;
(4)无水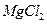 在熔融状态下,通电后会产生
在熔融状态下,通电后会产生 和
和 ,该反应的化学方程式为:
,该反应的化学方程式为:
。

 已知某白色混合物粉末中含有 Al2 (SO4)3、Na2SO4、NH4HCO3、NH4Cl、KCl五种物质中的两种。请完成下述探究混合物组成的实验
已知某白色混合物粉末中含有 Al2 (SO4)3、Na2SO4、NH4HCO3、NH4Cl、KCl五种物质中的两种。请完成下述探究混合物组成的实验 限选仪器、用品与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、酒精灯、火柴、试管夹;紫色石蕊试纸;1mol·L-1硝酸、1mol·L-1盐酸、1mol·L-1NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。
限选仪器、用品与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、酒精灯、火柴、试管夹;紫色石蕊试纸;1mol·L-1硝酸、1mol·L-1盐酸、1mol·L-1NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。 Ⅰ、初步探究
Ⅰ、初步探究 取适量混合物于烧杯中,用蒸馏水完全溶解,得到无色透明溶液A;取少量A于试管众,滴加稀硝酸,有无色气泡产生,继续滴加稀硝酸至溶液中不再产生气泡,得到无色透明溶液B。
取适量混合物于烧杯中,用蒸馏水完全溶解,得到无色透明溶液A;取少量A于试管众,滴加稀硝酸,有无色气泡产生,继续滴加稀硝酸至溶液中不再产生气泡,得到无色透明溶液B。 (1)上述实验证明:该混合物中肯定含有(名称),肯定不含有
(1)上述实验证明:该混合物中肯定含有(名称),肯定不含有 (化学式)
(化学式) Ⅱ、进一步探究
Ⅱ、进一步探究 (2)为了进一步确定该混合固体的组成,需要进行实验1或实验1、2,完成下表:
(2)为了进一步确定该混合固体的组成,需要进行实验1或实验1、2,完成下表:
| 实验操作 |
预期现象和结论 |
实验1:取少量溶液B于试管中,加入少量 Ba(NO3)2溶液,振荡,静置观察。 |
|
实验2: |
两个学习小组用下图装置探究乙二酸(HOOC—COOH)受热分解的部分产物。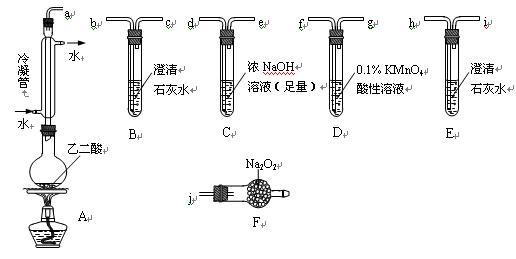
(1)甲组:
①按接口顺序:a—b—c—d—e—f—g—h连接装置进行实验。B中溶液变浑浊,证明分解产物有____________;装置C的作用是________________________;E中溶液变浑浊,D中的现象是________________________,证明分解产物有____________。
②乙二酸受热分解的化学方程式为____________________________________________。
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要反应的化学方程式为________________________________________________。
②从A~F中选用装置进行实验,证明甲组通入D的气体能否与Na2O2反应。
最简单的装置接口连接顺序是____________________________________;实验后用F中的固体进行验证的方法是____________________________________(可另选试剂)。
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示。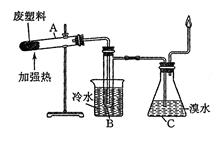
加热聚丙烯塑料得到的产物如下表:
| 产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
| 质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
(1)试管A中的最终残余物为________;在试验中大试管管口倾斜向上的原因是___________。
(2)试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有_____种。
(3)锥形瓶C中观察到的现象是_______________;经溴水充分吸收再干燥后,剩余两种气体的成份为____________,其平均相对分子质量为_____________。