已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) == 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
(2)C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ•mol-1
(3)H2(g) +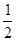 O2(g) == H2O(l) △H3=-285.8kJ·mol-1
O2(g) == H2O(l) △H3=-285.8kJ·mol-1
则反应2 C(s)+2H2(g) +O2(g) == CH3COOH(l)的△H为( )
| A.-488.3 kJ·mol-1 | B.-244.15 kJ·mol-1 |
| C.+488.3 kJ·mol-1 | D.+244.15 kJ·mol-1 |
空气吹出法是工业规模海水提溴的常用方法,流程如下:
下列说法不正确的是:
A.步骤①中发生的主要反应为 |
| B.步骤②③的目的是富集溴元素 |
| C.物质X 为HBrO |
| D.空气吹出法用到了溴易挥发的性质 |
已知:
下列实验方案,不能达到相应实验目的的是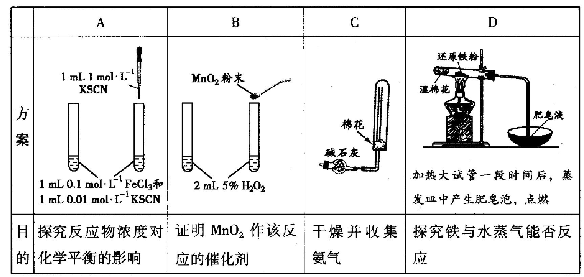
利用点滴板探究氨气的性质(如右图所示)。实验时向NaOH 固体上滴几滴浓氨水后,立即用表面皿扣住点滴板。下列对实验现象的解释正确的是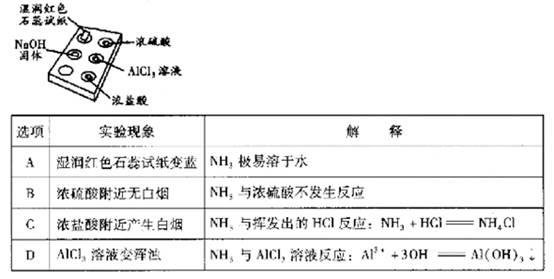
肼(N2H2 )是火箭常用的高能燃料,常温下为液体,其球棍模型如下图所示。肼能与双氧水发生反应: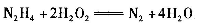 。用NA表示阿伏伽德罗常数,下列说法正确的是
。用NA表示阿伏伽德罗常数,下列说法正确的是
| A.标准状况下,11.2LN2 中含电子总数为5 NA |
| B.标准状况下,22.4LN2 H4中所含原子总数为6 NA |
| C.标准状况下, 3.2gN 2H4中含有共价键的总数为0.6 NA |
| D.若生成3.6gH2 O,则上述反应转移电子的数目为0.2 NA |