可逆反应A(?)+aB(g) 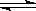 C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示。下列说法不正确的是( )
C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示。下列说法不正确的是( )
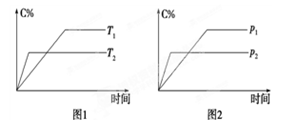
| A.若a=2,则A为液态或固体 |
| B.该反应的正反应为放热反应 |
| C.T2>T1,P2>P1 |
| D.其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大 |
元素性质呈周期性变化的决定因素是
| A.元素原子半径大小呈周期性变化 | B.元素的相对原子质量依次递增 |
| C.元素原子核外电子排布呈周期性变化 | D.元素的最高正化合价呈周期性变化 |
下列表示电子式的形成过程正确的是:
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
| X |
Y |
|
| Z |
W |
A.原子半径: W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.气态氢化物的稳定性:Z>W
D.W的单质能与水反应,生成一种具有漂白性的物质
下列各组化合物中,化学键类型完全相同的是
| A.CaCl2和 Na2S | B.Na2O 和Na2O2 | C.CO2和CaO | D.HCl和NaOH |
已知X、Y、Z都是第三周期元素,且核电荷数依次增大,X的最高价氧化物对应水化物为强碱,Z的原子半径在第三周期(除稀有气体外)最小。据此判断下列说法不正确的是
| A.X是ⅠA元素,Z是VIIA元素 |
| B.X、Y、Z三种元素的最高化合价逐渐减小 |
| C.Z的最高价氧化物对应的水化物是强酸 |
| D.X、Z形成的化合物是离子化合物 |