人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3—),它维持血液的pH稳定。已知在人体正常体温时,反应H2CO3 HCO3—+H+的平衡常数Ka=10—6.1,正常血液中[HCO3—]:[H2CO3]≈20:1,则关于血液缓冲体系的判断正确的是( )
HCO3—+H+的平衡常数Ka=10—6.1,正常血液中[HCO3—]:[H2CO3]≈20:1,则关于血液缓冲体系的判断正确的是( )
| A.正常人血液的pH约为7.4 |
| B.当过量的碱进入血液中时,发生的反应只有HCO3—+OH—→CO32—+H2O |
| C.血液中存在[HCO3—]+[OH—]+2[CO32—]=[H+]+[H2CO3] |
| D.正常人血液内不会存在以HCO3—/CO32—为主的缓冲体系 |
已知X、Y、Z、W四种短周期主族元素在周期表中相对位置如图所示,下列说法不正确的是
| X |
Y |
| Z |
W |
A.Y原子形成的简单离子半径一定比X原子形成的简单离子半径小
B.W的原子序数可能是Y的原子序数的3倍
C.W的气态氢化物的稳定性一定比Y的强
D.若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性
要组装一套实验室利用液体和液体反应制备气体的装置,现设计了如下的五步操作,正确的程序是
①将蒸馏烧瓶固定在铁架台上
②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网
③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集装置中
④检查装置的气密性(利用固定装置微热的方法检查气密性)
⑤在蒸馏烧瓶中装好分液漏斗,连接好导气管
| A.②①⑤④③ | B.④②①⑤③ |
| C.②①⑤③④ | D.①⑤④②③ |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
| A.分子式为C7H6O5 |
| B.分子中含有2种官能团 |
| C.可发生加成和取代反应 |
| D.在水溶液中羧基和羟基均能电离出H+ |
欲检验CO2气体中是否含有SO2、HC1,进行如下实验:
①将气体通入酸化的AgNO3溶液中,产生白色沉淀a;
②滤去沉淀a,向滤液中加入Ba(NO3)2溶液,产生白色沉淀b。
下列说法正确的是
| A.沉淀a为AgC1 | B.沉淀b为BaCO3 |
| C.气体中含有SO2 | D.气体中没有HC1 |
对常温下pH=3的CH3COOH溶液,下列叙述不正确的是
A.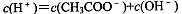 |
| B.加入少量CH3COONa固体后,c(CH3COO—)降低 |
| C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/L |
| D.与等体积pH =11的NaOH溶液混合后所得溶液显酸性 |