下列各溶液中,微粒物质的量浓度关系正确的是( )
A.0.1 mol·L-1Na2CO3溶液中c(OH-)=c(HC )+c(H+)+c(C )+c(H+)+c(C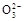 ) ) |
B.0.1 mol·L-1(NH4)2SO4溶液中:c(S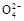 )>c(N )>c(N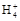 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
C.0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(OH-)>c(HC )>c(H+) )>c(H+) |
| D.0.1 mol·L-1Na2S溶液中:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) |
在1-氯丙烷和2-氯丙烷分别与NaOH的醇溶液共热的反应中,两反应
| A.产物相同 | B.产物不同 |
| C.碳氢键断裂的位置相同 | D.碳氢键断裂的位置不同 |
丙烯醇(CH2=CH—CH2OH)可发生的化学反应有
①加成②氧化③燃烧④加聚⑤取代
| A.只有①②③ | B.①②③④ |
| C.①②③④⑤ | D.只有①③④ |
已知分子式为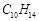 的有机物,只含一个取代基,可与液溴在铁粉的作用下反应生成一溴代物,则此烃的结构有
的有机物,只含一个取代基,可与液溴在铁粉的作用下反应生成一溴代物,则此烃的结构有
| A.2种 | B.3种 | C.4种 | D.5种 |
A、B两种有机物组成的混合物,当混合物的质量相等时,无论A、B以何种比例混合,完全燃烧时产生的CO2的质量都相等,一定符合这一条件的组合有:
①同分异构体 ②同系物 ③具有相同的最简式 ④含碳的质量分数相同
其中正确的是
A. ①②③ B. ①③④ C. ②③④ D. ①②③④
某气态烃1 mol最多和2 mol氢气发生加成反应,所得产物又能与10 mol氯气发生取代反应,最后得到一种只含碳、氯元素的化合物,则原气态烃为
| A.2-辛炔 | B.丙烯 | C.2-丁炔 | D.2-戊炔 |