某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用:
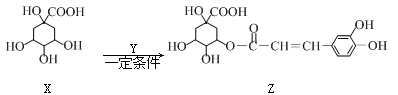
下列有关叙述中不正确的是( )
| A.Z结构中有4个手性碳原子 |
| B.Y的分子式为C9H8O4 |
| C.1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH |
| D.Z与浓溴水既能发生取代反应又能发生加成反应 |
根据表中信息判断,下列选项不正确的是
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4… |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO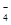 … … |
Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO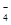 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠(NaClO3)的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O – 2e → SO42- + 4H+; (2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:Cl2 + 2e → 2Cl-。在(1)和(2)反应中均会生成产物X,则X的化学式为
| A.NaClO | B.NaClO4 | C.HClO | D.ClO2 |
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.3 mol |
| B.n(Na+)∶n(Cl-)可能为7∶3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1 |
某溶液中含有AlO2-、SO 、SO
、SO 、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
A.SO |
B.Na+ | C.AlO2- | D.SO |
在恒容密闭容器中通入X并发生反应:2X(g) Y(g);
Y(g); H="Q" kJ·mol-1。温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是( )
H="Q" kJ·mol-1。温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是( )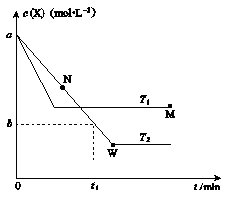
| A.该反应进行到M点放出的热量于小进行到W点放出的热量 |
B.T2下,在0~t1时间内,v(Y)=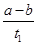 mol·L-1·min-1 mol·L-1·min-1 |
| C.M点的正反应速率v正大于N点的逆反应速率v逆 |
| D.M点时再加入一定量X,平衡后X的转化率减小 |