乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
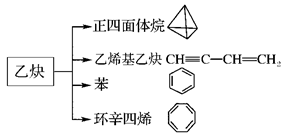
(1)正四面体烷的二氯取代产物有________种。
(2)关于乙烯基乙炔分子的说法正确的是________。
| A.能使酸性KMnO4溶液褪色 |
| B.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应 |
| C.乙烯基乙炔分子内含有两种官能团 |
| D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同 |
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子发生加聚反应的化学方程式为
(4)写出与苯互为同系物且一氯取代产物只有两种的物质的结构简式
(举两例):__________________、__________________。
有下列各组物质:
| A.O2和O3; | B.126C和136C; | C.冰醋酸和乙酸; | D.甲烷和庚烷;E.CH3-CH2-CH2-CH3和CH3CH(CH3)CH3; F.淀粉和纤维素。 |

 (1)互为同位素的是(2)互为同素异形体的是
(1)互为同位素的是(2)互为同素异形体的是 (3)互为同分异构体的是(4)同一物质是
(3)互为同分异构体的是(4)同一物质是 (5)互为同系物的是
(5)互为同系物的是
咖啡酸苯乙酯(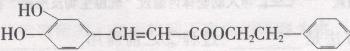 )是一种天然抗癌药物,在一定条件下能发生如下转化:
)是一种天然抗癌药物,在一定条件下能发生如下转化: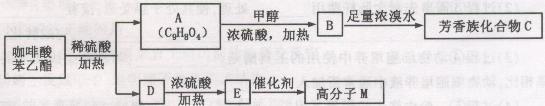
请填写下列空白:
(1)D分子中的官能团是;
(2)高子M的结构简式是;
(3)写出A→B反应的化学方程式;
(4)B→C发生的反应类型有;
(5)A的同分异构体有很多种,其中,同时符合下列条件的同分异构体有种。
①苯环上只有两个取代基②能发生银镜反应
③能与碳酸氢钠溶液反应④能与氯化铁溶液发生显色反应
有机物W(C3H6O3)能与NaHCO3反应,分子中含有四种活动性不同的氢原子,个数比为3∶1∶1∶1。
(1)W的结构简式是 。
(2)W的工业合成路线如下图所示:
已知:Ⅰ.A、B、C、D与W分子中含有相同碳原子数;
Ⅱ.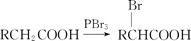
①写出A的结构简式是 ;
②B与新制Cu(OH)2反应的化学方程式是 ;
③D在NaOH水溶液中反应的化学方程式是 ;
④C的同分异构体中,能够与Ag(NH3)2OH溶液反应的有 种。
(3)工业上也可以用下图所示合成路线生产W:
已知:
请在合成路线框图中填入相应有机物的结构简式。
(4)W在一定条件下,反应生成丙交酯(C6H8O4)(含六元环结构),该反应的化学方程式是(有机物写结构简式)。
丙交酯在一定条件下聚合生成聚丙交酯(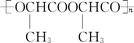 ),聚丙交酯经抽丝可制成手术缝合线,在人体内可自动缓慢降解为W。聚丙交酯在体内降解的化学方程式是
),聚丙交酯经抽丝可制成手术缝合线,在人体内可自动缓慢降解为W。聚丙交酯在体内降解的化学方程式是
。
已知:①R—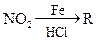 —
—
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图: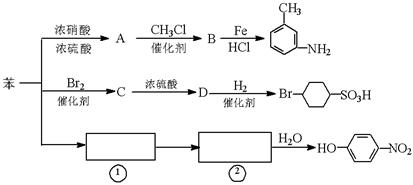
(1)A转化为B的化学方程式是_______________________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________________,②____________________________。
(3)B在苯环上的二氯代物有种同分异构体。
(4)有机物 的所有原子(填“是”或“不是”)在同一平面上。
的所有原子(填“是”或“不是”)在同一平面上。
氧化还原反应和离子反应是中学化学中最为重要的两大反应,试根据要求完下列问题:
(1)过量CO2与NaOH溶液反应的化学方程式:;
(2)用过量氨水吸收SO2的离子反应方程式:;
(3)实验室制取AI(OH)3的离子反应方程式:;