(8分) 2011年5月1日,我国实施“醉驾入刑”的新规,引起西园中学化学探究小组的注意,并设计如图实验,对人酒后呼出的气体与空气组成进行比较(不比较水蒸气).

【查阅资料】重铬酸钾溶液与乙醇反应,溶液由黄色变成浅绿色.
【提出假设】
猜想1:呼出的气体中含有乙醇;
猜想2:呼出的气体中 含量比空气的低;
猜想3:呼出的气体中 含量比空气的高。
【实验方案】
(1)按如图装置取气,得空气、呼出气体样品分别于A、C集气瓶中,取多瓶气样备用.
(2)图中澄清石灰水的作用是 .
(3)请填写空格
| 实验步骤 |
预期现象和结论 |
| ①向C集气瓶中伸入燃着的木条 |
火焰 ,证明猜想 成立 |
| ②同时向A、C集气瓶中加入等量的 |
若C集气瓶中 ,且较明显,证明猜想3成立 |
| ③分别向A、C集气瓶中加入少量重铬酸钾溶液 |
若 ,证明 . |
我市某化工厂排放的废液中含有硫酸铜和硫酸亚铁.某化学兴趣小组的同学取了适量的上述废液样品,将一定量锌粉加入样品中,充分反应后过滤,得到滤液A和固体B.
请回答下列有关问题:
(1)关于滤液A所含溶质的猜想中,不合理的是________(填写序号).
①猜想一:只有硫酸锌
②猜想二:硫酸锌、硫酸亚铁
③猜想三:硫酸锌、硫酸亚铁、硫酸铜
④猜想四:硫酸锌、硫酸铜
(2)设计简单实验,确定“猜想二”对应的固体B的成分:________________________________________.
(3)反应后析出金属的质量________(填“一定”或“不一定”)比参加反应的金属质量小.
为研究草酸亚铁晶体(FeC2O4•2H2O,相对分子质量是180)分解的产物,在实验室里称取一定量的草酸亚铁晶体,利用下列装置进行实验。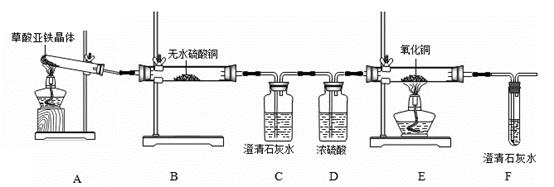
①实验过程中观察到B中白色无水CuSO4变成蓝色,C、F中澄清石灰水变浑浊,则E中现象是 (9) (填实验现象)。分解产物中有CO气体,还有 (10)。
②若该实验过程中E装置内有6.4g铜生成,计算有多少物质的量的氧化铜参加了反应?(写出反应的化学方程式,列出计算步骤!)
(11)写方程式:
(12)计算步骤:
③为验证CO的性质,收集装置D后的气体于集气瓶中,将点燃的木条伸入集气瓶中(如右图),在此过程中的实验现象是(13)(选填编号)。
A.木条熄灭 B.木条继续燃烧
C.瓶口产生淡蓝色火苗 D.发生爆炸
④进行上述实验时,先点燃A处的酒精灯,一段时间后再点燃E处的酒精灯,原因是(14)。
⑤若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加如图所示的洗气瓶,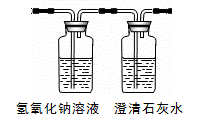
其中氢氧化钠溶液中发生的反应方程式是:(15) ;
澄清石灰水起到的作用是:(16)。
为了探究二氧化锰是否对氯酸钾的分解起了催化作用,经查阅资料得知:氯酸钾的熔点为356℃,加热到400℃可观察到缓慢放出气泡。实验仪器如下: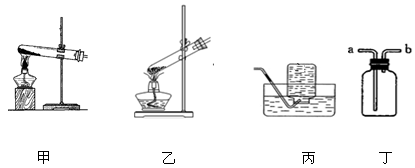
①实验设计如下,请你补充完成实验报告。
| 实验步骤 |
加热时间(分钟) |
实验现象 |
| 1.将二氧化锰单独放入试管中加热,将带火星的木条放在试管口 |
10 |
木条无变化 |
| 2.将氯酸钾单独放入试管中加热,将带火星的木条放在试管口 |
5 |
木条复燃 |
| 3.将 (1) ,将带火星的木条放在试管口 |
1 |
木条复燃 |
②该实验方法称为 (2),第二步实验中,某同学选用装置乙加热,你认为是否正确?理由是 (3)。
③写出第三步实验中发生的化学反应方程式 (4)。
④图“丙”中除导管外,另两个玻璃仪器的名称为(5)、(6);若用装置“丁”收集氧气,则导出气体的导管口是(7)(填写编号“a”或“b”)。
⑤实验室制取氧气还可用双氧水作为原料,比较用氯酸钾为原料的制取方法,用双氧水作原料的方案突出的优点是(8)(填写选项编号)
A.不需要加热,操作简单
B.通过分液漏斗加液,有利于连续操作
C.节约药品
D.可以使用启普发生器,使制取更方便
(10分)在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量M溶液于试管中,向其中滴加 |
猜想①正确,碳酸钠与其反应的化学方程式为 |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:_____;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中,滴入几滴稀盐酸 |
没有气体产生 |
“猜想一”不成立 |
他们的实验结论是否正确?,理由是.
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 |
实验现象 |
实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCI2溶液,B中加入溶液 |
若A中产生白色沉淀,B中没有沉淀 |
“猜想一”成立 |
| “猜想二”成立 |
||
| “猜想三”成立 |
通过学习我们知道,在化学变化中物质发生了改变,但质量是否改变了呢?为此某校甲、乙两个兴趣小组对这个问题进行了探究,过程如下:
【提出问题】参加反应的反应物总质量与生成物总质量是否相等
【实验方案】甲、乙两个兴趣小组分别设计了如图所示的实验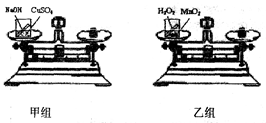
【进行实验】如图所示,甲小组把盛有适量NaOH溶液的小试管放入盛有CuSO4溶液的烧杯中,乙小组把盛有适量H2O2溶液的小试管放入盛有MnO2的烧杯中;然后将烧杯放到天平上调至平衡;接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡。
【实验现象】反应后,甲小组的天平指针指向刻度盘的(填“左边”、“右边”或“中间”),乙小组的天平指针指向刻度盘的右边。
【解释与结论】甲小组的结论为:,
化学方程式为CuSO4+2NaOH===Cu(OH)2↓+Na2SO4。乙小组的指针偏向右边是因为。
【反思与与评】比较两个小组的实验设计,你得到的启发是。