鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设鸡蛋壳中的其他物质不与盐酸反应)
(1)产生二氧化碳气体 g。
(2)计算10g该鸡蛋壳中碳酸钙的质量,要求写出完整的解题步骤。
实验室常用一定质量分数的过氧化氢溶液制取氧气。某同学取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质量是34.4g。求:(1)生成氧气的质量。(2)该同学所用过氧化氢溶液中滴质质量分数。
制作“叶脉书签”需要l00g溶质质量分数为10%的氢氧化钠溶液。请问:
(I)配制时需要氢氧化钠固体的质量是g.水的质量是g;
(2)若用20%的氢氧化钠溶液和水配制,需要20%的氢氧化钠溶液质量是g。
(10南京市22).(12分)某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为▲g,水的体积为▲mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的▲盘,称量其质量。然后 ▲(按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是▲.
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)如图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。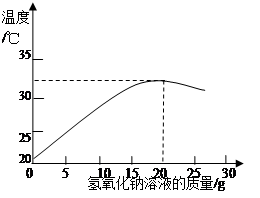
①根据曲线判断,当加入氢氧化钠溶液的质量为▲时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为▲(写化学式)。
③试计算该稀盐酸中溶质的质量分数(请写出计算过程)▲
(10天津市27).某食品加工厂生产的酱油中氯化钠的质量分数为16%,该厂日产酱油15t。试计算该厂每月(按30天计)消耗氯化钠的质量。
某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”),其原理是向氨化的饱和氯化钠溶液通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O=NH4CI+NaHCO3。该方法不但可以制得纯碱(将NaHCO3进一步处理即可得到纯碱),还得到优质氮肥氯化氨。试通过计算回答下列问题:
⑴氯化氨中氮元素的质量分数为(计算结果保留0.1%)
⑵实验中得到碳酸氢钠8.4g,求参加反应的氨气质量为多少?
⑶课外活动小组为了这次模拟实验,准备了8.8g二氧化碳,制取这些二氧化碳需要消耗质量分数为10%的稀盐酸的质量为多少?