下列关于离子的检验说法正确的是( )
| A.向某溶液中滴入足量盐酸,如观察到无色无味的气体产生,且能使澄清石灰水变浑浊,即证明溶液中必定有CO32- |
| B.向某无色溶液中加入BaCl2溶液,有白色沉淀出现,再加入稀盐酸,沉淀不消失,无法证明溶液一定含有SO42- |
| C.向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无NH4+ |
| D.如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素 |
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是()
| A.O点溶液中所含溶质的化学式为NaOH、Na2CO3 |
| B.常温下,a点溶液显碱性 |
| C.标准状况下,通入CO2的体积为4.48L |
| D.原NaOH溶液的物质的量浓度为2.5mol/L |
下列关于离子检验的叙述正确的是( )
| A.向FeCl2、NaI的混合溶液中加入硫氰化钾溶液,再滴加少量氯水,溶液没有变为红色,说明还原性:Fe2+<I- |
| B.检验AlNH4(SO4)2溶液中的NH4+:取样于试管中,向溶液中加入少量NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体 |
| C.检验Na2SO3和Na2SO4的混合溶液中的SO42-:先加足量稀硝酸,再加氯化钡溶液 |
| D.验证碳酸钠溶液显碱性是CO32-导致的:先加酚酞试液,溶液变红,再加硫酸溶液,红色褪去 |
下列情境中溶液的导电能力没有经过“先减弱后增强”变化的是(忽略溶液体积的变化)( )
| A.向饱和硫化氢溶液中持续通入SO2 |
| B.向硫酸铝溶液中持续加入氢氧化钡固体 |
| C.向Ca(HCO3)2溶液中滴加澄清石灰水至过量 |
| D.向氯化铁溶液中持续通入SO2 |
利用下列实验装置能完成相应实验的是( )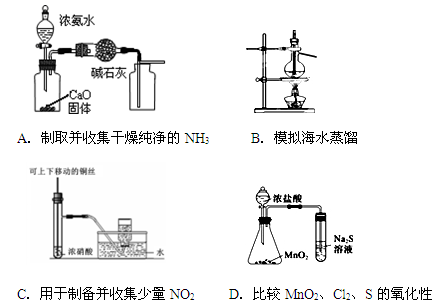
除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法不正确的是()
| 选项 |
待提纯的物质 |
选用试剂 |
操作的方法 |
| A |
FeCl2溶液(FeCl3溶液) |
铁粉 |
过滤 |
| B |
Al2O3(Fe2O3) |
NaOH溶液和CO2 |
溶解、过滤、过滤 |
| C |
Cl2(HCl) |
饱和食盐水 |
洗气 |
| D |
Na2CO3固体(NaHCO3固体) |
—— |
加热至质量不再变化 |