要配制下列含有四种不同阴、阳离子的溶液,其中能配制成功的是( )
| A.Fe2+、OH-、NO3-、Cl- | B.Ca2+、H+、Cl-、HCO3- |
| C.Mg2+、Al3+、Cl-、SO42- | D.Na+、Ca2+、NO3-、CO32- |
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是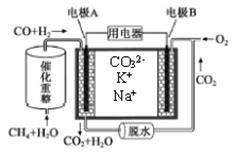
A.反应CH4+H2O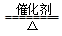 3H2+CO,每消耗1molCH4转移12mol e- 3H2+CO,每消耗1molCH4转移12mol e- |
| B.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
| C.电池工作时,CO32-向电极B移动 |
| D.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
下列说法正确的是
| A.氯化钠固体不导电,所以氯化钠是非电解质 |
| B.向纯水中加入碳酸钠能使水的电离平衡正向移动,水的离子积增大 |
C.如图研究的是铁的吸氧腐蚀,实验中红色首先在食盐水滴的中心出现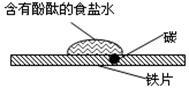 |
| D.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) 的△H<0 △S<0 |
下列对化学反应的认识正确的是
| A.化学反应过程中,分子的种类和数目一定发生改变 |
| B.如果某化学反应的△H和△S均小于0,则反应一定能自发进行 |
| C.化学反应过程中,一定有化学键的断裂和形成 |
| D.所有的吸热反应一定要在加热的条件下才能进行 |
下列离子方程式与所述事实相符且正确的是
| A.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++C1O-+H2O=MnO2↓+C1-+2H+ |
| B.用稀硝酸清洗做过银镜反应的试管:Ag+NO3-+4H+=Ag++NO↑2H2O |
| C.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4C1- |
D.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液:2C1-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
关于下图所示的原电池,下列说法正确的是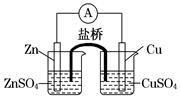
| A.电子沿着盐桥从锌电极流向铜电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.电流从锌电极通过电流计流向铜电极 |
| D.铜电极上发生的电极反应是2H++2e-===H2↑ |