高纯度晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场 “革命”。它可以按下列方法制备:
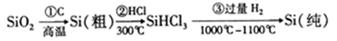
下列说法正确的是( )
A.步骤①的化学方程式为:SiO2+C Si+CO2↑ Si+CO2↑ |
| B.步骤①②③中每生成或反应1mol Si,转移4mol电子 |
| C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 |
| D.SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
| A.反应生成的大量白烟是氯化钠晶体 |
| B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 |
| C.钠着火燃烧产生苍白色火焰 |
| D.若在棉球外沿滴一滴紫色石蕊溶液,可根据其颜色变化判断氯气是否被碱液完全吸收 |
下列反应的离子方程式中,不正确的是
| A.氯化铜溶液与铁粉反应:Cu2++Fe═Fe3++Cu |
| B.NaHSO4溶液与氢氧化钠溶液反应:OH﹣+H+═H2O |
| C.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42﹣═BaSO4↓ |
| D.碳酸钙与盐酸反应:CaCO3+2H+═H2O+CO2↑+Ca2+ |
金属加工后的废切削液中含2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2
第二步:NH4NO2=N2↑+2H2O
下列对第二步反应的叙述中正确的是
①NH4NO2只是氧化剂 ②NH4NO2只是还原剂 ③NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化⑤NH4NO2既是氧化剂又是还原剂.
| A.①③ | B.①④ | C.②③④ | D.③④⑤ |
在反应3Cl2+6KOH=KClO3+5KCl+3H2O中,氧化剂与还原剂的质量比为
| A.2:1 | B.5:1 | C.1:2 | D.1:5 |
下列有关物质用途的叙述中,错误的是
| A.液氨常被用作制冷剂 |
| B.可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 |
| C.为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 |
| D.已知3Cl2+2NH3═N2+6HCl,工业上可用浓氨水检查氯气管道是否漏气 |