钙是人体必须的常量元素,每日必须摄入足够量的钙.目前市场上的补钙药剂很多,下图是某种品牌的补钙药品的部分说明书.请回答下列问题:
(1)
中钙元素的质量分数为.
(2)若每片钙片的质量为0.5
,则钙片中钙元素的质量分数为.
(3)如果按用量服用,每天摄入钙元素的质量为
.
将8.0g氢氧化钠完全溶于水形成溶液,向其中加入一定质量的硫酸铜溶液,恰好完全反应,所得混合物总质量为109.8g(铜的相对原子质量为64).计算:
(1)反应产生沉淀的质量.
(2)反应后所得溶液的溶质质量分数.
为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取10
石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图(见图).
(1)碳酸钙完全反应用去稀盐酸的质量为
.
(2)该石灰石样品中碳酸钙的质量分数为.
(3)当盐酸和石灰石恰好完全反应,所得溶液中溶质质量分数是多少?(规范写出计算过程)
四川泡菜深受人们喜爱.
(1)家庭用含
94%的袋装食用盐配制泡菜水,要求泡菜水中
的质量分数为18.8%,则1000
水中需加袋装食用盐
.
(2)要测定某泡菜水中
的含量,取70
澄清的泡菜水(密度为1.1
),加入足量的
溶液,充分反应后滤出沉淀,洗净烘干后称得其质量为28.7
.假设泡菜水中的其他物质均不与
溶液反应,求这种泡菜水中
的质量分数.(计算结果保留l位小数,无计算过程不给分)
向100
稀
溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的
溶液,所得沉淀质量与加入
溶液质量关系如图所示.请回答: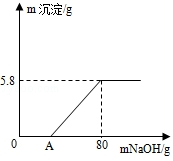
(1)
段无沉淀产生,请写出反应的化学方程式;
(2)加入镁粉的质量为
;
(3)求产生氢气的质量是多少
?(写出计算过程,保留小数点后一位).