设NA为阿伏伽德罗常数的值。下列说正确的是
| A.高温下,0.2molFe与足量稀硫酸反应反应,生成的H2分子数目为0.3NA |
| B.78g过氧化钠中含阴离子数为2 NA |
| C.C2H4和N2组成的42g混合气体中原子的个数为3 NA |
D.5NH4 NO3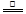 2HNO3+4N2↑+ 9H2O反应中,生成28gN2时,转移的电子数目为3.75NA 2HNO3+4N2↑+ 9H2O反应中,生成28gN2时,转移的电子数目为3.75NA |
向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化。坐标系中a、b、c三条曲线分别对应的离子是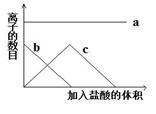
| A.Na+ CO32- HCO3- |
| B.Cl- Na+ CO32- |
| C.Na+ HCO3- CO32- |
| D.Na+ CO32- H+ |
下列反应的离子方程式正确的是
| A.向溴水中加入NaOH溶液:Br2 +2 OH-= BrO-+ Br- |
| B.少量H2SO4滴入Ba(OH)2溶液中:Ba2+ + OH-+ H+ + SO42-= BaSO4↓+ H2O |
| C.过量NaHCO3溶液滴入NaHSO4溶液中:HCO3-+ H+ = H2O + CO2↑ |
| D.在漂白粉溶液中通入过量的CO2:Ca2+ + 2ClO-+ CO2+ H2O = CaCO3↓+ 2HClO |
根据下列反应判断有关物质的还原性由强到弱的顺序正确的是
①
②
③
A. |
B. |
C. |
D. |
下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
| A.Mg2+、Na+、SO42-、Cl— | B.K+、CO32-、Cl—、NO3— |
| C.NH4+、Na+、SO42-、NO3— | D.Na+、K+、NO3—、SO32— |
只给出下列甲和乙中对应的物理量,不能求出物质的量的是
| A.甲:物质中的粒子数;乙:阿伏加德罗常数 |
| B.甲:标准状况时的气体摩尔体积;乙:标准状况时的气体体积 |
| C.甲:固体的体积;乙:固体的密度 |
| D.甲:溶液中溶质的物质的量浓度;乙:溶液体积 |