常温下,浓度均为0.1mol/L CH3COOH溶液和HCN溶液的pH分别为m和n(1<m<n)。下列叙述中不正确的是
| A.常温下,pH相同的CH3COOH溶液和HCN溶液分别加水稀释相同的倍数时,前者pH变化小 |
| B.等温下,等浓度的CH3COONa和NaCN溶液pH,后者大 |
| C.HCN溶液和NaOH溶液不等体积混合后一定存在C(H+)―C(OH-)=C(CN-)―C(Na+) |
| D.溶液中由水电离出的c(H+),前者是后者的10m-n倍 |
下列各种说法中正确的是……( )
| A.凡没有单质参加的化合反应一定是非氧化还原反应 |
| B.有单质参加的反应一定是氧化还原反应 |
| C.凡有盐参加的反应都是复分解反应 |
| D.置换反应一定是氧化还原反应 |
由2-氯丙烷制取少量的1,2-丙二醇需要经过下列哪几步反应( )
| A.加成→消去→取代 | B.消去→加成→水解 |
| C.取代→消去→加成 | D.消去→加成→消去 |
为了检验溴乙烷中含有溴元素,有以下操作的合理顺序是()
①加AgNO3溶液②加NaOH溶液③加热④加蒸馏水⑤加硝酸至溶液显酸性
| A.②①③⑤ | B.②④⑤③ | C.②③⑤① | D.②①⑤③ |
下列卤代烃,在一定条件下,能发生消去反应的是()
| A.CH3Cl |
| B.CH3—CHBr—CH3 |
C.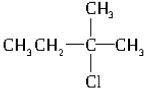 |
D.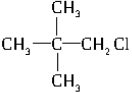 |
为了使氯乙烷的水解反应进行得比较完全,水解时需加入()
| A.NaCl | B.NaHSO4 | C.HCl | D.NaOH |