某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示。下列判断正确的是
| A.原溶液中一定含有Na2SO4 |
| B.原溶液中一定含有的阴离子是OH-,CO32-,SiO32-,AlO2- |
| C.反应后形成的溶液溶质为NaCl |
| D.原溶液中含有CO32-与AlO2-的物质的量比为1:2 |
下列物质中含有共价键的离子化合物是
| A.CaCl2 | B.Ba(OH)2 | C.H2O | D.H2 |
下列各组微粒中,核外电子总数相等的是
| A.Na+和Li+ | B.CO和CO2 | C.H2O和H3O+ | D.NO和CO |
元素周期表是学习化学的重要工具,右图是元素周期表中的一格,从该图中,我们获取的相关信息中错误的是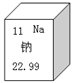
| A.该元素的名称是钠 | B.该元素的原子序数为11 |
| C.该元素在地壳中的含量为22.99% | D.该元素的元素符号为Na |
已知X、Y、Z为同周期三种原子序数相连的短周期元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
| A.原子序数:Z>Y>X | B.非金属活泼性:Y<X<Z |
| C.原子半径:X>Y>Z | D.气态氢化物的稳定性:HX>H2Y>ZH3 |
周期表中17号元素的原子37Cl和6号元素的原子13C的原子相比较,前者的下列数据是后者的4倍的是
| A.中子数 | B.最外层电子数 | C.电子层数 | D.次外层电子数 |