碳及其化合物在人类生产、生活中的应用非常广泛。“低碳生活”不再只是一种理想,更是一种值得期待的生活方式。
(1)已知:①2CH4(g)+3O2(g)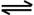 2CO(g)+4H2O(l) △H1=-1214.6kJ/mol
2CO(g)+4H2O(l) △H1=-1214.6kJ/mol
②2CO(g)+ O2(g)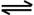 2CO2(g) △H2=-566kJ/mol,
2CO2(g) △H2=-566kJ/mol,
则甲烷与氧气反应生成二氧化碳和液态水的热化学方程式为 。
(2)已知在恒温恒压下密闭容器的可逆反应CH4(g)+ H2O(g)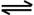 CO(g)+3H2(g)
CO(g)+3H2(g)
①该可逆反应一定达到平衡的标志是 。
| A.v(CH4)正=3v(H2)逆 |
| B.水蒸气的浓度与一氧化碳的浓度相等 |
| C.平均相对分子质量不随时间的变化而变化 |
| D.密度不随时间的变化而变化 |
②该可逆反应在不同条件下,测得CH4转化率随时间变化如图所示,与实验a相比,b的实验条件是 。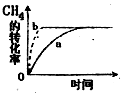
(3)将不同物质的量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g) 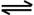 CO2(g)+H2(g);△H得到如下三组数据:
CO2(g)+H2(g);△H得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| H2O |
CO |
CO2 |
CO |
|||
| 1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
D |
t |
①实验1中以v(H2)表示的反应速率为 。
②实验2中的平衡常数是 (计算结果保留两位小数)。
③该反应的△H 0(填“>”或“<”)。
④若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),则a、b应满足的关系
是 (用含a、b的式子表示)。
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子核外电子排布图为______________________________;
(2)写出与H2O分子互为等电子体的微粒______________________(填2种);
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是___________;
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
(4)在冰晶体中,以一个水分子为中心,画出水分子间最基本的连接方式(水分子用结构式表示);
(5)下列是钾、碘、金刚石、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____,D晶体的空间利用率为。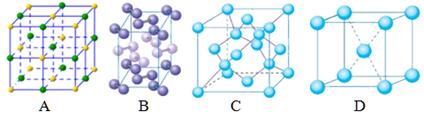
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| a |
b |
||||||||||||||||
| c |
d |
e |
|||||||||||||||
| f |
g |
||||||||||||||||
试回答下列问题(凡涉及的物质均用化学式表示):
(1)a的氢化物的分子构型为,中心原子的杂化形式为;d在空气中燃烧产物的分子构型为,中心原子的杂化形式为,该分子是(填“极性”或“非极性”)分子。
(2)b、d、e三种元素的氢化物中的沸点最高的是,原因是:。
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。此配合离子空间构型为,请写出生成此配合离子的离子方程式:。
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f3+ 的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为,该配合物的配体是、;
(5)c单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
c单质晶体中原子的配位数为。若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M。该晶体的密度为(用字母表示)。
根据要求完成下列问题:
(1)有以下物质:①SO2Cl2 ②C2H6 ③CS2 ④HClO ⑤H2O2
含有非极性键的非极性分子是___________;
以极性键相结合,具有直线型结构的非极性分子是___________;
以极性键相结合,具有四面体形结构的极性分子是___________;
以极性键相结合,具有V型结构的极性分子是___________;
(2)在S8、SiC、NaCl、C2H5OH中,能形成分子晶体的化合物是,含有氢键的晶体的化学式是,属于原子晶体的是,
四种物质形成的晶体熔点由高到低的顺序是>>>。
下图立方体中心的“o”表示SiC晶体中的一个硅原子,请在立方体的顶点用“●”表示出与之紧邻的碳原子。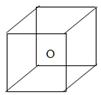
可以由下列反应合成三聚氰胺:CaO+3CCaC2+CO↑,CaC2+N2CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:______________________________________________________________________。
CaCN2中阴离子为CN,与CN互为等电子体的分子有N2O和________(填化学式),由此可以推知CN的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________________。
(3)三聚氰胺  俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸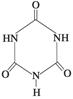 后,
后,
三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______________。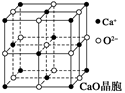
已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离 __________________(列出计算式)
CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是____________________。
天然气(主要成分甲烷)是一种清洁、高效的能源,现在许多城市家庭用于厨房使用的燃料已经由煤气(主要成分是H2和CO按体积比1︰1混合的气体混合物)换成了天然气;此外天然气也是很好的燃料电池的燃料,甲烷在燃料电池中的能量转换率可达到85%—90%。请回答下列问题:
⑴已知H2、CO和CH4的燃烧热分别是286kJ/mol、283 kJ/mol和890 kJ/mol,则反应2CH4(g)+3O2(g)=CO(g)+H2(g)+CO2(g)+3H2O(l)的反应热△H=。
⑵以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为:。随着反应的不断进行溶液的pH(填“增大”“减小”或“不变”)。
⑶如果以该燃料电池为电源、石墨作两极电解饱和食盐水,则该电解过程中阳极反应式为:;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12,则理论上消耗甲烷在标准状况下的体积为:mL。
⑷将⑶中电解结束后的溶液取出,向其中加入含有Mg2+和Fe2+的溶液甲,Mg(OH)2和Fe(OH)2同时生成,已知Mg(OH)2和Fe(OH)2在该温度下的溶度积常数分别是2×10—11和8×10—16,则甲溶液中Mg2+和Fe2+的浓度比为:。