为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,某学习小组设计了如图装置来进行实验。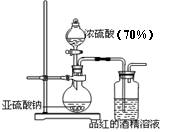
请回答下列问题:
(1)亚硫酸钠与浓硫酸反应的化学方程式是 。
为了探究干燥的SO2能不能使品红褪色,请指出设计的实验装置图中两个明显的不足:① ;② 。
(2)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是SO2直接导致。为此,SO2通过品红水溶液后,引起品红褪色的微粒可能是 。
(3)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,对此,他得出结论:使品红褪色的微粒是HSO3-、SO32-,不是H2SO3。乙同学认为他的结论不正确, 其理由是 。
(4)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红溶液各20mL加入两只小烧杯中,两只烧杯中同时一次性各加入20mL0.1mol/L的亚硫酸钠溶液和20mL0.1mol/L的亚硫酸氢钠溶液,发现加入亚硫酸钠溶液的品红褪色明显较快。小组同学分别比较了两种溶液中各微粒浓度与褪色快慢的关系,得出的结论是 ,理由是 。
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。①提出合理假设。
假设1:该漂白粉未变质,只含;
假设2:该漂白粉全部变质,只含;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
②设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 |
预期现象和结论 |
|
| ① |
取少量上述漂白粉于试管中, |
|
| ② |
||
| ③ |
磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4的废液)为原料来制备磁材氧化铁。

已知煅烧中的化学反应方程式为:FeCO3 → FeO + CO2↑,4FeO + O2 → 2Fe2O3
(1)用98%的H2SO4的配制500mL的20%的H2SO4,所需玻璃仪器是
| A.玻璃棒 | B.烧杯 | C.漏斗 | D.250mL容量瓶 |
E、500mL容量瓶 F、胶头滴管
(2)浓缩结晶后得到的晶体是(填化学式),A中溶质是;
此溶液中各离子的浓度比较大小为:。
(3)20%H2SO4和铁皮的作用分别是。
(4)检验滤液中含有NH4+的方法是
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示):
。
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连续装置,检查装置的气密性。
(2)将mg铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是:。点燃酒精灯一段时间后,B中可观察到的明显现象是。C中足量的酸性KMnO4溶液所起的作用是。D中盛放的试剂是。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
。
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,则铁碳合金中铁的质量分数为(写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是。
(5)经过大家的讨论,决定采用上图装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是(填写代号)。
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
喷泉是一种常见的现象,其产生的原因是存在压强差。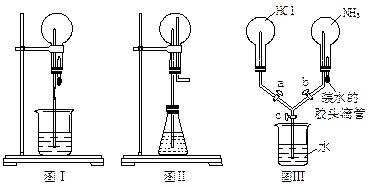
(1)图Ⅰ为化学教学中常用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
A. SO2和H2O B. CO2和NaOH溶液 C. NH3和H2O D. NO和H2O
(2)在图Ⅱ的锥形瓶中,分别加入足量的下列物质后,能产生喷泉的是
A. Cu与稀硫酸 B. Cu与稀硝酸 C. Al与浓硫酸 D. Fe与浓硝酸
(3)比较图Ⅰ和图Ⅱ两套装置,从产生喷泉的原理来分析,图Ⅰ是上部烧瓶内气体压强;图Ⅱ是下部锥形瓶内气体压强(填“增大”或“减小” )。
(4)某学生积极思考喷泉原理的应用,设计了如图Ⅲ所示的装置。
① 如果关闭活塞c,打开活塞a、b,再挤压胶头滴管。则可能出现的现象为。
② 在①操作的基础上,打开活塞c,产生的现象是。
某课外活动小组为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:
(1)甲装置中CO2与过量的NaOH反应的离子方程式。
(2)丙装置实验现象是,解释产生该实验现象的原因
。
(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中安全性存在问题,该方案是(填甲、乙或丙),原因是
。
(4)请设计一个实验检验生成的产物Na2CO3中的阴离子。(简述操作步骤、所用试剂、实验现象和结论。)
(5)实验室中若需用44.8 L(标准状态)CO2 ,现用含CaCO3 90%石灰石与足量的盐酸反应,至少需要这种石灰石 g