在离子浓度均为0.1 mol·L-1的下列溶液中,加入(通入)某物质后,离子反应先后顺序正确是
| 选项 |
实验操作 |
反应先后顺序 |
| A |
含Fe3+、Cu2+、H+的溶液中加入锌粉 |
Cu 2+、Fe3+、H+ |
| B |
含I-、S2-、Br-的溶液中不断通入氯气 |
S2-、I-、Br- |
| C |
含Cl-、Br-、I-的溶液中逐滴加入AgNO3溶液 |
Cl-、Br-、I- |
| D |
含Al 3+、H+、NH4+ 的溶液中逐滴加入NaOH溶液 |
H+、NH4+、Al 3+ |
我国稀土资源丰富。下列有关稀土元素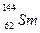 与
与 的说法正确的是
的说法正确的是
| A.二者互为同位素 |
| B.二者是同一种核素 |
| C.二者的质量数相同 |
| D.二者的核外电子数和中子数均为62 |
常温熔融盐又称常温离子液体(ionic liquid),1914年报道的第一种离子液体硝酸乙基铵〔(C2H5NH3)NO3〕,其熔点为12℃。已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是
| A.该离子液体中含的氨分子 |
| B.硝酸乙基铵水溶液呈碱性 |
C.硝酸乙基铵水解的离子方程式可表示为:C2H5NH3++2H2O C2H5NH2·H2O+H3O+ C2H5NH2·H2O+H3O+ |
| D.同温度下相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH小 |
下列化学方程式或离子方程式中,正确的是
A.用浓硫酸与4-溴-1-丁醇加热发生消去反应: |
B.水杨酸( )中加入NaHCO3溶液: )中加入NaHCO3溶液: +2HCO3-→ +2HCO3-→ +2CO2↑+2H2O +2CO2↑+2H2O |
| C.向CuSO4溶液中滴加过量的氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+ |
| D.用侯氏制碱法制得NaHCO3 : Na++NH3+CO2+H2O =NaHCO3↓+NH4+ |
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学设计了实验方案(见下表),将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
| 实验 试剂 |
甲 |
乙 |
丙 |
丁 |
| 4 mol·L-1H2SO4/mL |
20 |
V1 |
V2 |
V3 |
| 饱和CuSO4溶液/mL |
0 |
2.5 |
V4 |
10 |
| H2O/mL |
V5 |
V6 |
8 |
0 |
| 收集气体所需时间/s |
t1 |
t2 |
t3 |
t4 |
下列说法正确的是
| A.t1 < t2 < t3 < t4 | B.V4=V5=10 |
| C.V6="7.5" | D.V1<V2<V3<20 |
赫克反应、根岸反应和铃木反应已成为化学家们制造复杂化学分子的“精致工具”,在科研、医药和电子等领域已经广泛应用。下例是由铃木反应合成出来的一种联苯的衍生物:
下列叙述正确的是
| A.1 mol该联苯的衍生物在一定条件下最多可和7 mol H2发生加成反应 |
| B.该联苯的衍生物属于芳香烃 |
| C.该联苯的衍生物苯环上的一硝基取代产物有7种 |
| D.该反应为加成反应,且原子利用率达100% |