某研究性学习小组利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。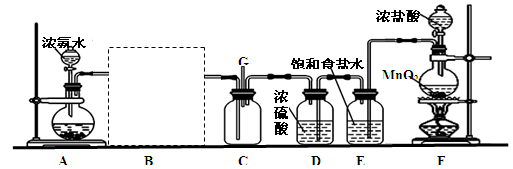
请回答下列问题:
(1)为了快速制备氨气,装置A中烧瓶内的固体可以是 (填序号)。
①二氧化硅
②过氧化钠
③生石灰
④氢氧化钠固体
⑤氯化钙
(2)请在B处虚线框内画上合适的装置图并注明所装试剂名称。
(3)装置F中发生反应的离子方程式为: 。
(4)装置D和E的位置 (填“能”或“不能”)调换,装置E的作用是: 。
(5)通入C装置的两根导管左边较长、右边较短,目的是: 。
(6)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出发生反应的化学方程式,并标出电子转移的方向和数目: 。
(7)从装置C的G处逸出的尾气可能含有污染环境的气体,如何处理? 。
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。

⑴写出下列仪器的名称:
①;②;④;
⑵仪器①~④中,使用时必须检查是否漏水的有。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有_____________,将仪器补充完整后进行的实验操作的名称为:__________。
(4)现需配制250 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是_________。
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: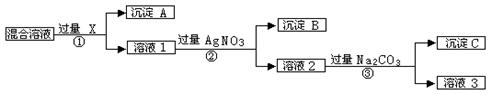
请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X _______,沉淀A:_______,沉淀B:__________。
⑵上述实验流程中加入过量的Na2CO3的目的是____________________________
⑶按此实验方案得到的溶液3中肯定含有_____________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的_________,之后若要获得固体NaNO3需进行的实验操作是___________________(填操作名称).
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。
确定CaCl2溶液是否过量的方法是____________________________________,
判断沉淀是否洗净的操作是____________________________________________。
(2)乙组:气体分析法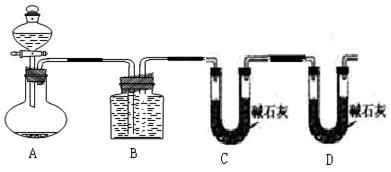
用如图装置进行实验,为了减少误差,分液漏斗中应该用____________溶液,B中应该用_____________________溶液,选用该溶液后实验结果还是不准,请问是_____________,(填“偏高”、“偏低”或“无影响”)原因是______________________________________。
(3)请你设计一个与甲、乙两组操作不同的实验方案,测定混合物中Na2CO3的含量。
方案:__________________________________。
用到的主要试剂:_____________________________________。
用到的玻璃仪器:_____________________________________(至少2件)
用18mol/L的浓硫酸配制100.00mL 1.00mol/L硫酸:
(1)用量筒量取浓硫酸的体积应为mL(保留一位小数),将浓硫酸缓缓倒入盛水的烧杯中后__ __(填“应该”或“不应”)用少量蒸馏水洗涤量筒2~3次并将洗涤溶液也倒入烧杯中。
(2)若实验仪器有:
| A.100mL量筒 | B.托盘天平 | C.玻璃棒 | D.50mL容量瓶 |
E.10mL量筒 F. 胶头滴管 G. 50mL烧杯 H. 100mL容量瓶
实验时应选用的仪器有(填入编号)。
(3)量取浓硫酸时,若俯视液面,则所配稀硫酸溶液浓度________定容时,若俯视液面,则所配溶液浓度 ____(填“偏高”、“偏低”或“无影响”);若不小心加水超过了容量瓶刻度线,应。
“碘钟”实验中,3I-+S2O42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
| ① |
② |
④ |
⑤ |
⑥ |
|
| c(I-)/mol·L-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
| c(S2O42-)/mol·L-1 |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
| t /s |
88.0 |
44.0 |
22.0 |
44.0 |
t2 |
回答下列问题:(1)该实验的目的是。
(2)显色时间t2=。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为(填字母)
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析上表数据,得出的结论是