下图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题: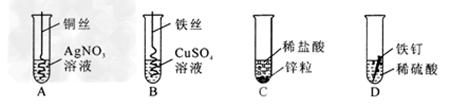
(1)描述A中的实验现象________________________________________________________.
(2)写出C中反应的化学方程式是________________________________________________.
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是___________(填序号);
(4)开始反应后D中溶液逐渐变为黄色,原因是____________________________________.
研究盐类物质的性质时,甲、乙、丙三位同学分别向NaHCO3溶液中滴加石灰水,均产生白色沉淀.他们分别设计实验方案,对自己过滤后的滤液中溶质的成分进行如下探究.
【实验准备】
用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 |
NaOH溶液 |
Na2CO3溶液 |
|
| 加入酚酞溶液 |
溶液变红 |
现象Ⅰ |
溶液变红 |
| 加入CuSO4溶液 |
产生气泡和蓝色沉淀 |
现象Ⅱ |
产生气泡和蓝色沉淀 |
| 加入CaCl2溶液 |
无明显变化 |
无明显变化 |
产生白色沉淀 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 |
澄清石灰水 变浑浊 |
澄清石灰水 无明显变化 |
澄清石灰水 无明显变化 |
表中的现象Ⅰ为 ;现象Ⅱ为产生蓝色沉淀,对应反应的化学方程式是 .
【查阅资料】
(1)氯化钙溶液显中性.
(2)滤液中所含的溶质有以下几种可能:①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH
【实验及分析】
甲同学:取少量滤液于试管中,滴加过量的稀盐酸,产生大量无色气泡,则滤液中的溶质是Na2CO3.
乙同学:取少量滤液于试管中,向其中通入少量CO2,产生白色沉淀,则滤液中的溶质是
NaOH和Ca(OH)2.
丙同学:分别取少量滤液于两支试管中,向一支试管中滴加CaCl2溶液,有白色沉淀产生;将另一支试管中的滤液加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3.
【反思与评价】
(1)老师认为乙、丙同学的实验方案和结论合理.
①丙同学的实验中,加入CaCl2溶液的目的是 .
②根据乙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是 .
(2)老师认为甲同学的实验方案和结论存在不足.丁同学通过以下实验帮助甲同学确认了滤液中溶质的成分.
| 实验操作 |
实验现象 |
实验结论 |
| ① ② |
① ② |
滤液中的溶质是Na2CO3和NaOH |
(3)结合此次探究活动,你认为下列说法正确的是 (填字母序号).
a.盐溶液可能显碱性
b.化学反应的产物与反应物的量有关
c.碱和盐反应一定生成另外一种碱和另外一种盐
d.判断溶液混合后的成分不仅要考虑产物,还要考虑反应物是否过量.
化学小组的同学用如图所示的装置探究二氧化碳的性质后,觉得探究很有意思,想继续探究.
[提出问题]反应后溶液中的溶质有什么?
[查阅资料](1)氢氧化钠与二氧化碳反应的化学方程式为 .
(2)在上述反应中,若二氧化碳过量,能发生如下反应:
Na2CO3+H2O+CO2=2NaHCO3
[猜想与假设]通过分析,小明做出如下猜想:
①含有NaOH和 Na2CO3;②含有Na2CO3和NaHCO3;
[实验探究]为确定反应后溶液的组成,同学进行了如下两项探究活动.
(1)对相关物质性质的研究.
| NaHCO3溶液 |
NaOH溶液, |
Na2CO3溶液 |
|
| 加入稀盐酸 |
产生气泡 |
无明显变化 |
产生气泡 |
| 加入饱和石灰水 |
溶液变浑浊 |
溶液变浑浊 |
现象I |
| 加入CaCl2溶液 |
无明显变化 |
溶液变浑浊 |
溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 |
澄清石灰水 变浑浊 |
澄清石灰水 无明显变化 |
澄清石灰水 无明显变化 |
上表中现象I对应的化学方程式为 .
(2)探究反应后溶液的成分.为确认反应后溶液的组成,小明设计了如下实验过程
| 实验步骤 |
操作 |
实验现象 |
实验结论 |
| ① |
取一定量反应后溶液放入试管中,滴加适量的CaCl2溶液. |
有沉淀产生 |
|
| ② |
将步骤①所得的混合物过滤,洗涤,并将滤渣分成两部分. |
||
| ③ |
向其中一份步骤②所得固体中滴加稀盐酸. |
有气泡产生. |
原溶液中含有 . |
| ④ |
取另一份步骤②所得固体, . |
. |
猜想1正确 |
[反思与评价]
(1)若想直接证明小明的另一个猜想不正确,在上述方案的基础上,应加做的实验是
.
(2)小伟提出,小明的猜想不完全,反应后溶液的组成还可能是 (有几种写几种).
实验课上,同学们用下图所示四种溶液探究与指示剂的作用.实验后进行废液处理,处理过程为:将A和B中液体混合,得到红色溶液E;将C和D中液体混合,得到废液F;将E和F放入烧杯中.
(1)向A中滴加无色酚酞溶液后,溶液颜色为 色.
(2)A和B混合后,溶液中一定没有 .
a.NaCl b.HCl c.NaOH
(3)C和D混合时发生反应的化学方程式为 .
(4)继续对烧杯中的废液成分进行如下探究.
【提出问题】烧杯废液中含有什么物质?
【查阅资料】碳酸钠溶液呈碱性;CaCl2溶液呈中性.
【初步分析】通过分析上述实验现象,烧杯中的废液除酚酞和水外还一定含有 .
【进行实验】请设计实验验证可能含有的物质
| 实验操作 |
现象与结论 |
(5)为实现绿色排放(溶液呈中性),应对废液再进行的操作是 .
用如图所示装置分别进行两个实验(已知:氯化钙溶液呈中性).
(1)打开止水夹,向Ⅰ中液体加入一种黑色固体、Ⅱ中液体加入一种白色固体.Ⅰ和Ⅱ中均有气泡出现,且Ⅱ中液体内出现燃烧现象.
①写出燃烧反应的化学方程式 .
②请说明Ⅱ中出现燃烧的原因 .
(2)打开止水夹,向Ⅰ中液体加入一小块固体.Ⅰ和Ⅱ中均有气泡出现,且Ⅱ中液体出现浑浊现象.关闭止水夹,发现Ⅱ中液面上升,溶液由浑浊变澄清.
①请说明溶液由浑浊变澄清的原因 .
②若实验后Ⅱ中澄清液中的溶质由一种或两种物质组成,为检验其成分,应该进行的实验操作是
.
化学小组同学在课外读物中看到:“Na2O2广泛应用于潜艇的呼吸供氧和CO2的去除.”他们决定探究CO2与Na2O2反应的产物.提出猜想CO2与Na2O2反应可能生成O2和Na2CO3.查阅资料
①Na2O2是一种淡黄色固体,常温下与CO2、H2O等物质反应,反应的化学方程式分别为:2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑.
②CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液中.
③Na2O2与稀盐酸反应时,生成NaCl、H2O和O2.
实验过程同学们在老师的指导下利用如下图所示装置(部分夹持仪器已略去)进行实验
(1)实验时上述仪器正确的连接顺序为m接 (填接口字母).
(2)检验有氧气产生的方法是将 放在接口 处(填接口字母);证明有氧气产生的实验现象是 .
(3)检验有Na2CO3生成的方法是 .
(4)使气体通过D装置的原因是 .