下列有关二氧化硫的说法中,错误的是
| A.二氧化硫能漂白某些物质,说明它具有氧化性 |
| B.二氧化硫的水溶液能使紫色石蕊溶液变红,说明它能与水反应生成H2SO3 |
| C.将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原性 |
| D.实验室可用氢氧化钠溶液处理含有二氧化硫的尾气 |
下列解释不科学的是
| A.“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用生成了可溶性的Ca(HCO3)2的缘故。 |
| B.长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成“负压”的缘故。 |
| C.严格地讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收。 |
| D.“雨后彩虹”、“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的知识有关。 |
某种酯的结构可表示为:CmH2m+1COOCnH2n+1,其中m+n=5,该酯的一种水解产物经催化氧化可转化成它的另一种水解产物,则原来的酯是
| A.丙酸乙酯 | B.乙酸乙酯 | C.丁酸甲酯 | D.丙酸丙酯 |
有一系列有机化合物按下列顺序排列:CH3CH=CHCHO、CH3CH=CHCH=CHCHO、CH3(CH=CH)3CHO、……,在该系列有机物中,分子中含碳元素的质量分数的最大值最接近于
| A.95.6% | B.92.3% | C.85.7% | D.75.0% |
分子式为C9H20的烷烃,它的同分异构体中有些只能由一种相应的烯烃经催化加氢得到,C9H20的同分异构体中具有这样结构的异构体共有
| A.1种 | B.2种 | C.3种 | D.4种 |
如右图,向A充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应,X(g)+Y(g)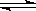 2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是
A.反应速率:v(B)>v(A)B.A容器中X的转化率为80%
C.平衡时的压强:PB=2PAD.平衡时Y体积分数:A<B