(1)下图是工业氮气和氢气合成1mol氨气过程中能量变化示意图,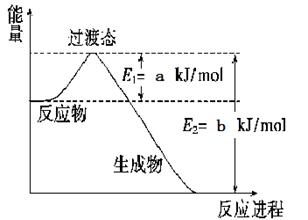
请写出该反应的热化学方程式 。
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=C02(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:△H=____ 。
(3)将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如下图所示。
正极上发生的电极反应为___
阴极上发生的电极反应为___
(4)如图是甲烷燃料电池原理示意图,回答下列问题: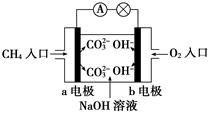
①电池的负极是________(填“a”或“b”)极,负极的电极反应式是__ _。
②电池工作一段时间后电解质溶液的pH______(填“增大”、“减小”或“不变”)
常温下,有下列三种溶液:①0.1 mol/L NH4Cl②0.1 mol/L NH4HCO3③0.1 mol/L NH4HSO4
请根据要求填写下列空白:
(1)溶液①呈性(填“酸”、“碱”或“中”),其原因是:
(用离子方程式表示)
(2)比较溶液②、③中c(NH4+)的大小关系是②③﹝填“>”、“<”或“=”)
甲醇是一种优质的液体燃料,CO和CO2均可用于合成甲醇。
目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g) +3H2(g) =CH3OH(g)+H2O(g)△H1
(1)已知:2CO(g) +O2(g) =2CO2(g)△H2
2H2(g)+O2(g) =2H2O(g)△H3
则CO(g) + 2H2(g)  CH3OH(g)的△H=。
CH3OH(g)的△H=。
(2)由CO合成甲醇时,CO在不同温度下的平衡转化率与压强的关系如下图所示。
该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
(3)
一定温度下,向2L密闭容器中加入1mol CH3OH (g),发生反应:CH3OH(g)  CO(g) + 2H2(g),H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(CH3OH)=。
CO(g) + 2H2(g),H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(CH3OH)=。
该温度下,CO(g) + 2H2(g)  CH3OH(g)的平衡常数K=。
CH3OH(g)的平衡常数K=。
相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则是原来的2倍。
a.平衡常数 b.CH3OH的平衡浓度 c.达到平衡的时间 d.平衡时气体的密度
(4)以CH3OH为燃料(以KOH溶液作电解质溶液)可制成CH3OH燃料电池。
①充入CH3OH的电极为极;
②负极反应的电极反应式为。
.Ⅰ、研究性学习小组进行SO2的制备及性质探究实验,装置如下图(a为活塞,加热及固定装置已略去)
①连接仪器、、加药品后,打开a,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是:
。
③从品红溶液中观察到的现象说明SO2具有性。
④高锰酸钾溶液中的实验现象是。
Ⅱ、上述实验中NaOH溶液用于吸收剩余的SO2生成Na2SO3,Na2SO3是抗氧剂。向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色。
(1)写出在碱性中Br2氧化Na2SO3的离子方程式
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO42-和Br-的实验报告(步骤可增减)。
限选试剂:2 mol·L-1 HCl;1 mol·L-1 H2SO4;l mol·L-1 BaCl2;l mol·L-1 Ba(NO3)2;
0.1 mol·L-1 AgNO3;CCl4;新制饱和氯水。
| 编号 |
实验操作 |
预期现象和结论 |
| 步骤① |
有白色沉淀生成,证明待测液中含SO42-。 |
|
| 步骤② |
||
| 步骤③ |
||
| …… |
M5纤维是美国开发的一种超高性能纤维,下面是以对二甲苯为原料合成M5纤维的合成路线(有些反应未注条件):请回答:
(1)写出对二甲苯的含苯环结构的所有同分异构体的结构简式_________________、_____________________、_____________________。
(2)写出合成M5的单体F的结构简式:____________________________。
(3)反应类型:A→B_______________________,B→C_________________________。
(4)写出化学方程式(注明反应条件):
B→C______________________________________________________,
D→E______________________________________________________。
下列物质能导电的是属于电解质的是,属于非电解质的是。
①水银②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸
⑥氨气 ⑦蔗糖 ⑧氯气 ⑨液态氯化氢 ⑩硫酸溶液