微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,负极反应为:Zn+2OH--—2e-==ZnO+H2O;正极反应为:Ag2O+H2O+2e-==2Ag+2OH-,根据反应式,判断下列叙述正确的是
| A.在使用过程中,电池正极区溶液的pH增大 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是正极,Ag2O是负极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
关于下列各装置图的叙述中,正确的是
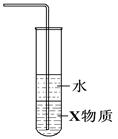

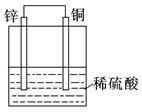
①②③④
| A.实验室用装置①制取氨气 |
| B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| C.装置③可用于制备氢氧化亚铁并观察其颜色 |
| D.装置④是原电池,锌电极为负极,发生还原反应 |
除去下列物质中少量杂质的方法正确的是
| A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 |
| B.除去NO2中混有的NO:用水洗气 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
下列说法正确的是
A.甲烷和苯 都能发生取代反应 都能发生取代反应 |
| B.乙醇和乙酸都能与氢氧化钠发生中和反应 |
| C.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 |
| D.淀粉、油脂、蛋白质都属于天然高分子化合物 |
在化学学习与研究中类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中,不正确的是
| A.CO2不能与CaCl2溶液反应,则SO2也不能与CaCl2溶液反应 |
| B.金属钠着火不能用CO2扑灭,则金属钾着火也不能用CO2扑灭 |
| C.乙烯能使酸性KMnO4溶液褪色,则丙烯也能使酸性KMnO4溶液褪色 |
| D.Al(OH)3能与NaOH溶液反应,则Al(OH)3也能与氨水反应 |
以NA表示阿伏 加德罗常数,下列说法正确的是
加德罗常数,下列说法正确的是
| A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA |
| B.28gCO中所含的原子数为2NA |
C.0.1mol/LNa2CO3溶液中,含有CO32— 数为0 .1NA .1NA |
| D.标况下,22.4L苯的分子数为NA |