(10分,每空2分)水的电离平衡曲线如图所示。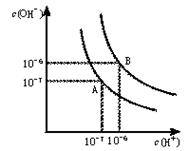
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将pH=8的NaOH溶液与pH=5的稀盐酸混合,并且保持100℃的恒温,欲使混合溶液pH=7,则NaOH与盐酸的体积比为 。
(3)普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是 。
(4)室温时,Mg(OH)2(S) Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全 (指Mg2+的浓度等于10-5mol/L) 时,溶液的pH=_______。已知25℃时Ksp[Mg(OH)2]=1.0×10-11,
Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全 (指Mg2+的浓度等于10-5mol/L) 时,溶液的pH=_______。已知25℃时Ksp[Mg(OH)2]=1.0×10-11,
通常采用将钠与亚硝酸钠(NaNO2)在空气中共热的方法制取氧化钠,反应的另一产物为N2,则该反应的化学方程式为_______________,该反应的氧化剂是________,被氧化的元素是___________。
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如下图所示,由此确定,原溶液中含有的阳离子是: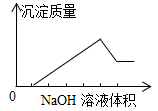
| A.Mg2+、Al3+、Fe2+ |
| B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ |
| D.只有Mg2+、Al3+ |
在里或下能够导电的化合物叫做电解质,电解质溶液之所以能够导电,是由于它们在溶液里发生了,产生了。酸与碱发生中和反应的实质是
在化学反应中,如果反应前后元素化合价发生变化,就一定量有转移,这类反应就属于反应,元素化合价升高,表明该元素的原子电子,含有该元素的物质发生反应,这种物质是剂,元素化合价降低,表明该元素的原子电子,含有该元素的物质发生反应,这种物质是剂。
在0.3 molNH3中约含NH3的分子数是个原子数是个这些NH3中所含的分子数与mol的水分子数相等,与mol的硫酸分子数相等。