氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:
Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.AlN中氮的化合价为+3 |
| C.上述反应中,每生成1 mol AlN需转移3 mol电子 |
| D.AlN的摩尔质量为41 g |
下图装置可用于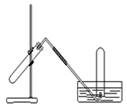
| A.用NH4Cl与浓NaOH溶液反应制NH3 | B.用Cu与稀HNO3反应制NO |
| C.加热NaHCO3制CO2 | D.用MnO2与浓HCl反应制Cl2 |
下列反应属于取代反应的是
| A.苯 → 环己烷 | B.乙酸 → 乙酸乙酯 |
| C.乙烯 → 乙醇 | D.乙醇 → 乙醛 |
XY2是由短周期元素形成的化合物,Y-比X2+多一个电子层,它与氩原子的电子层结构相同。下列有关叙述不正确的是
| A.Y是第ⅦA族元素 | B.X是第二周期元素 |
| C.Y-与X2+的最外层电子数相同 | D.化合物XY2的化学键为离子键 |
下列离子方程式书写正确的是
| A.FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- |
| B.稀盐酸与小苏打溶液混合:CO32-+2H+=CO2↑+H2O |
| C.鸡蛋壳溶于食醋:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.AlCl3溶液加入过量的氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
下列关于有机化合物的说法正确的是
| A.乙醇和乙酸都存在碳氧双键 |
| B.甲烷和乙烯都可以与氯气反应 |
| C.高锰酸钾可以氧化苯和甲烷 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |