配制50g一定溶质质量分数的氯化钠溶液,实验步骤如下:
(1)计算:氯化钠质量和水的体积(水的密度:1.0g/mL).
(2)称量:如图所示(右盘无砝码)称量的氯化钠质量为________g.
量取:选择________(填“30”“50”或“100”)mL的量筒准确量取________水.
(3)溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解,配得的氯化钠溶液中溶质的质量分数为________.
(4)装瓶、贴标签:请填写图所示标签.
【反思】
(5)上述实验过程中,用量筒量取水时,若按图方式进行读数,将导致所配溶液的溶质质量分数________(填“偏大”“不变”或“偏小”).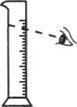
根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间能否发生反应,将表中内容补充完整.
| 氢氧化钠溶液 |
氯化钠溶液 |
碳酸钾溶液 |
硝酸钡溶液 |
|
| 稀硫酸 |
能反应 |
不能反应 |
能反应 |
|
| 判断依据 |
有水生成 |
没有水、气体、沉淀生成 |
【提出问题】稀硫酸与氢氧化钠溶液的反应没有观察到明显现象,是否真的发生了反应?
【实验方案】小丽同学设计实验方案进行探究,证明氢氧化钠溶液与稀硫酸发生了反应,请你和她一起完成实验报告.
| 实验操作 |
实验现象 |
| ①向试管中加入约2稀氢氧化钠溶液,滴加2滴溶液 |
|
| ②向①所得液体中滴加过量稀硫酸 |
【实验结论】稀硫酸与氢氧化钠溶液发生了反应;
【实验拓展】小丽结合所学知识,认为初中常见的酸碱之间一定能发生复分解反应,她判断的依据是.
小明学习了酸碱指示剂后,根据探究活动的提示,在家中自制紫甘蓝汁酸碱指示剂.小明在家中找到了如下用品:废塑料盒、捣蒜用的杵、筷子、纱布、白酒、紫甘蓝,并用这些用品完成了实验.
第一步:制紫甘蓝汁.
①将紫甘蓝在废塑料盒中捣烂,加入浸泡一段时间;
②将①中得到的不溶物与液体分离,(写具体做法),得到了自制的紫甘蓝汁.
第二步:小明欲用制得的紫甘蓝汁测出家中炉具清洁剂和厕所清洁剂的酸碱性,先上网查得下列资料,如表所示:
| 在不同溶液中的颜色变化 |
||
| 盐酸 |
氢氧化钠溶液 |
|
| 紫甘蓝汁 |
红色 |
黄色 |
第三步:小明取少量厕所清洁剂放入废塑料盒中,加入紫甘蓝汁,发现溶液变为红色,得出厕所清洁剂显性;小明又取少量炉具清洁剂放入废塑料盒中,加入紫甘蓝汁,发现溶液变为色,得出厨房清洁剂显碱性;小明认为紫甘蓝汁可以替代实验室中的石蕊溶液做酸碱指示剂.
图1是实验室制取气体的常用装置
(1)实验室常用过氧化氢溶液和二氧化锰制取氧气,若要控制反应速率,应选择的发生装置是(填字母,下同);若要收集较为纯净的氧气,应选择的收集装置是;写出该反应的化学方程式.
(2)实验室用大理石和稀盐酸反应制取二氧化碳,写出该反应的化学方程式;若用图2装置干燥二氧化碳,气体应从(填"
"或"
")端通入;若用图2装置检验二氧化碳,写出发生反应的化学方程式;
(3)碱式碳酸铜是一种绿色粉末,受热条件下会分解成三种氧化物,若用实验证明加热碱式碳酸铜有新物质生成,应将干燥的碱式碳酸铜放入装置进行反应,观察到,证明生成物之一为水.
将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
(1)
点处溶液的溶质是;
(2)请写出
段发生反应的化学方程式;
(3)
点处溶液的
7(填"
"、"
"或"
").
化肥对提高农作物的产量具有重要作用,在硝酸钾( )、硫酸铵[ ]、尿素[ ]三种化肥中,属于复合肥的是,不能与碱性物质混合施用的是.