请计算下列各题,并探究其关的规律.
(1)①要使100g10%的硝酸钾溶液变成20%的硝酸钾溶液,可将溶液中的水分蒸发掉_______g.②要使200g含水99%的氯化钠溶液变成含水量为98%的溶液,需蒸发掉水的质量为__________g.
[规律]要将mga%的某种物质的溶液的溶质质量分数增大一倍(即变成2a%),需要蒸发掉水的质量应等于________g(假设此过程中无溶质析出)。
(2)①要使100g10%的硝酸钾溶液变成5%的硝酸钾溶液,可向溶液中加入水的质量为______g.
②在溶质质量分数为24%的氯化钾溶液中加入120g水后,溶液中溶质的质量分数变为原来的一半,则原溶液中溶质的质量为________g.
[规律]要将mg2a%的某物质的溶液的溶质质量分数减小一半(即变为a%),则需加入水的质量为_______g.
(3)①将100g10%的酒精溶液与100g30%酒精溶液充分混合后,所得溶液中酒精的质量分数是________.
②要用80%的硫酸溶液和10%的稀硫酸配制500g45%的硫酸溶液,则需80%的硫酸溶液的质量为_______g,需10%的稀硫酸的质量为______g.
[规律]将m%和n%的两份同种溶质的溶液等质量混合,则所得溶液中溶质的质量分数为_____.
某班同学设计下图所示的实验来探究碳酸钙与盐酸反应是否遵守质量守恒定律。
(1)甲同学按图1的方案实验。称量好后,先把烧杯倾斜后又将烧杯放回托盘,看到烧杯中产生大量气泡。实验结束时天平指针将(选填“偏左”、“偏右”、“指向中间”)
(2)乙同学认为用有气体参加或生成的反应来验证质量守恒定律时,应在密闭的体系中进行,按图2的方案实验。氢氧化钠吸收二氧化碳方程式为CO2+2NaOH=Na2CO3+H2O。调节天平平衡后,挤压胶头滴管逐滴滴入盐酸,发现天平始终保持平衡,则试管内发生反应的化学方程式为。老师认为用该方案来验证也不合适,你认为理由是。
(3)丙同学听从老师意见按图3的方案实验。将注射器内吸满了盐酸,全部挤入锥形瓶中,一段时间后发现天平指针突然大幅向右偏转,你认为可能原因是。若不考虑注射器活塞自重和摩擦力作用,锥形瓶容积为750mL,注射器实际容积为12mL,吸取1mL的稀盐酸做该实验,欲确保实验成功,理论上所用盐酸的质量分数最大为。(保留小数0.01%)(假设稀盐酸密度为1.0g/mL,二氧化碳密度为2.0g/L)
某校化学研究性学习小组通过实验研究高炉炼铁的化学原理,设计了如下实验装置:
(1)已知HCOOH(甲酸) CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是(填小写字母序号);
CO↑+H2O,根据该反应制取CO,A处应选用的气体发生装置是(填小写字母序号);
(2)装置中仪器①的名称是;装置B内所盛放浓硫酸作用是干燥CO,D装置的作用为(用化学方程式表示)。
(3)①实验开始时应先点燃(填“A”或“C”)的热源;②反应前后C装置玻璃管内物质颜色变化是;③C装置玻璃管内发生反应的化学方程式为;④检验C中的产物是否为铁的方法是;⑤待C装置玻璃管内物质冷却后再停止通CO的目的是。
(4)该装置有一个明显的缺陷,改进的方法为。
(5)用高炉炼铁得到含杂质的铁10g(杂质不溶于水,也不参加反应)与100g稀硫酸恰好完全反应,滤去杂质,得到滤液质量为108.1g,则含杂质的铁中铁的质量分数为。
使用红磷燃烧的方法测定空气中氧气的含量:
(1)写出红磷在空气中燃烧的化学方程式。
(2)在集气瓶中加入少量水,并将水面上方空间分成5等份,如图装置所示。待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此可知氧气约占空气总体积的。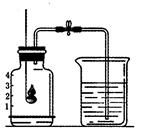
(3)实验后发现测定空气中氧气含量偏高,造成这种结果的可能原因是:(填一种即可)。
(4)已知五氧化二磷溶于水且化学性质与二氧化碳相似,反应完毕后振荡集气瓶再滴入紫色石蕊溶液,溶液变色。
完成下列变化的化学方程式,并按要求填空。
(1)常温下铝和氧气发生反应:;其基本反应类型是:反应。
(2)镁在空气中燃烧:;夹持镁条的仪器是:。
(3)炼铁高炉内焦炭与二氧化碳反应:;该反应属于(选填“放热”或“吸热”)反应。
(4)铁粉浸入硫酸铜溶液中:;其基本反应类型是:反应。
(5)碳酸氢铵晶体受热分解:;碳酸氢铵应如何保存:。
科学家经过多年研究证明,很多同学爱吃的某些小包装零食中,含一定量的有毒、有害、致病的化学物质。某些油炸食品中含有致癌物质丙烯酰胺,丙烯酰胺的化学式为C3H5ONx。回答下列问题:
(1)碳元素和氧元素的质量比是(填最简整数比)。
(2)丙烯酰胺的相对分子质量为71,则x的数值为。