根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
/ |
Fe3+ Br2 |
Cl- |
| ② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
由2—氯丙烷为主要原料制取1,2—丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
| A.加成—消去—取代 | B.消去—加成—取代 |
| C.取代—消去—加成 | D.取代—加成—消去 |
下列有机物的命名正确的一组是 ()
A.二溴乙烷 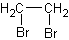 |
B.3-乙基-1-丁烯  |
C.2-甲基-2,4-己二烯 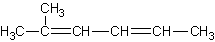 |
D.2-甲基-1-丙醇 |
下列说法中错误的是
| A.若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 |
| B.C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 |
| C.CO2与SiO2晶体熔化时,所克服的微粒间相互作用相同 |
| D.短周期元素离子aXm+和bYn-具有相同的电子层结构,则a>b |
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
| A.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
| D.若Y的最高正价为+m,则X的最高正价一定为+m |
R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝对值等于电子层数;Q元素的原子比R元素的原子多2个核外电子,则下列叙述中肯定不正确的是
| A.原子半径:R>Q | B.R和Q可形成离子化合物 |
| C.R和Q可形成非极性分子RQ2 | D.R和Q可形成共价化合物RQ3 |