用酸性氢氧燃料电池电解苦卤水 (含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。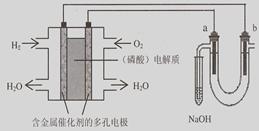
下列说法中正确的是
| A.电池工作时,负极反应式为:H2 +2 OH――2e-=2H2O |
| B.电解时,a 电极周围首先放电的是Br-而不是Cl-,说明当其它条件相同时前者的还原性强于后者 |
| C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D.忽略能量损耗,当电池中消耗0.32g O2 时,b 极周围会产生0.04g H2 |
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y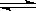 2Z,其平衡常数为1600(mol/L) -2
2Z,其平衡常数为1600(mol/L) -2
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
在一密闭容器中,反应aA(气)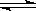 bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的60%,则
bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的60%,则
| A.平衡向逆反应方向移动了 |
| B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 |
| D.a>b |
在一密闭容器中进行以下可逆反应:M(g)+N(g) P(g)+2L,在不同的条件下P的百分含量P%的变化情况如下图,则该反应
P(g)+2L,在不同的条件下P的百分含量P%的变化情况如下图,则该反应
| A.正反应放热,L是固体 |
| B.正反应放热,L是气体 |
| C.正反应吸热,L是气体 |
| D.正反应放热,L是固体或气体 |
用Pt作电极,电解串联电路中分装在甲、乙两个烧杯中的200mL 0.3mol·L-1的NaCl溶液和300mL 0.2mol·L-1的AgNO3溶液,当产生0.56L(标况)Cl2时,停止电解,取出电极,将两杯溶液混合,混合液的pH为(混合后溶液体积为500mL)。
| A.1.4 | B.5.6 | C.7 | D.12.6 |
已知反应:①2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/mol
下列结论正确的是
| A.碳的燃烧热110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀醋酸与稀NaOH溶液反应的中和热为57.3 kJ/mol |
| D.稀盐酸与稀NaOH溶液反应的中和热为57.3 kJ/mol |