向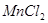 溶液中加入过量难溶电解质
溶液中加入过量难溶电解质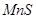 ,可使溶液中含有的
,可使溶液中含有的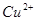 、
、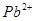 、
、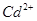 等金属离子转化为硫化物沉淀,从而得到纯净的
等金属离子转化为硫化物沉淀,从而得到纯净的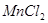 。下列分析正确的是
。下列分析正确的是
A.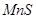 具有吸附性 具有吸附性 |
B.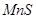 有还原性,将 有还原性,将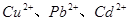 还原后除去 还原后除去 |
C.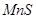 溶液度大于 溶液度大于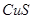 、 、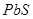 、 、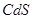 |
D.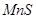 与 与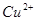 反应的离子方程式是 反应的离子方程式是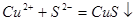 |
常温下,下列溶液中各微粒的物质的量浓度关系正确的是( )
| A.浓度为0.1 mol/L CH3COOH与0.1 mol/L CH3COONa混合后溶液呈弱酸性,则c(CH3COOH>c(Na+)>c(CH3COO-) |
| B.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ |
| C.NaHCO3溶液:c(OH-)-c(H+)=c((HCO3-)+2c(H2CO3) |
| D.等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO) + c(ClO-)= c(HCO3-) + c(H2CO3) + c(CO32-) |
X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时, X和W可形成化合物,该化合物0.1mol/L的水溶液pH为1,下列说法正确的是 ( )
| A.Z、R、W形成的单核离子核外电子数相等 |
| B.R元素的最高价氧化物的水化物酸性最强 |
| C.原子半径:X<Y<Z<R<W |
| D.X、Z分别与Y可形成原子个数比为1:1或2:1的化合物 |
下列有关热化学方程式的叙述正确的是 ( )
| A.已知2H2 (g)+O2(g)=2H2O(g ) △H=﹣483.6kJ/mol,则H2的燃烧热为△H=﹣241.8kJ/mol |
| B.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热 的热化学方程式为:NaOH(aq) + HCl(aq) ═ NaCl(aq) + H2O(l) △H=﹣57.4kJ/mol |
| C.反应NH3(g) + HCl(g)=NH4Cl (s) △H<0 ,该反应在任何温度下都可自发进行 |
| D.已知C(s) + O2(g)=CO2(g) △H1;C(s) + 1/2 O2(g) ═ CO(g) △H2,则△H1>△H2 |
下列有机物结构与性质分析正确的是( )
A.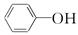 与 与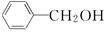 是同系物 是同系物 |
| B.乙酸乙酯(CH3COOCH2CH3)的核磁共振氢谱出现三组峰,且峰面积之比为3:2:3 |
| C.分子式为C4H10的有机物一氯代物共有8种 |
D.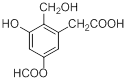 含氧官能团有4种 含氧官能团有4种 |
下列有关命名的说法正确的是( )
A.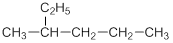 主链上的碳原子数是5 主链上的碳原子数是5 |
B.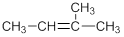 名称是3甲基2丁烯 名称是3甲基2丁烯 |
C.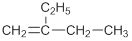 加氢后可以得到3-甲基戊烷 加氢后可以得到3-甲基戊烷 |
D.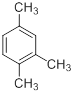 的名称是1, 3, 4-三甲基苯 的名称是1, 3, 4-三甲基苯 |