下列有关化学用语表示正确的是
A.氢氧化钠的电子式: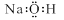 |
B.Cl-的结构示意图: |
C.2-丁醇的结构简式: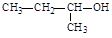 |
| D.碳酸的电离方程式:H2CO3=2H++CO32- |
在实验室中,通常将金属钠保存在()。
| A.水中 | B.煤油中 | C.四氯化碳中 | D.汽油中 |
常温下,对下列四种溶液的叙述正确的是( )
| 编号 |
① |
② |
③ |
④ |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸溶液 |
盐酸 |
| pH |
11 |
11 |
3 |
3 |
A、②、③两溶液相比,溶液中水的电离程度不同
B、四种溶液分别加水稀释10倍,pH变化最大的是①和③
C、①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D、①、④两溶液按一定体积比混合,所得溶液中离子浓度的关系不存在:c(H+)>c(Cl-)>c(OH-)>c(NH4+)
在容积相同且固定不变的四个密闭容器中,进行同样的可逆反应:2A(g)+B(g) 3C(g)+2D(g),起始时四个容器所盛A、B的量分别为:甲:2 mol A,1 mol B;乙:1 mol A,1 mol B;丙:2 mol A,2 mol B;丁:1 mol A,2 mol B。在相同温度下建立平衡时,A、B的转化率大小关系正确的是( )
3C(g)+2D(g),起始时四个容器所盛A、B的量分别为:甲:2 mol A,1 mol B;乙:1 mol A,1 mol B;丙:2 mol A,2 mol B;丁:1 mol A,2 mol B。在相同温度下建立平衡时,A、B的转化率大小关系正确的是( )
A、A的转化率:甲<丙<乙<丁 B、A的转化率:甲<乙<丙<丁
C、A的转化率:甲<乙=丙<丁 D、B的转化率:甲>丙>乙>丁
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的
是()
| A.燃料电池工作时,负极反应为:H2 – 2e-= 2H+ |
| B.若要实现铁上镀铜,则a极是铁,b极是铜 |
| C.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下当电池中消耗H2 22.4 L(标准状况)时,a极析出铜64 g |