下列化学用语描述中正确的是
A.含18个中子的氯原子的核素符号: |
B.比例模型 可以表示CO2分子或SiO2分子 可以表示CO2分子或SiO2分子 |
C.HCO3-的电离方程式为:HCO3-+ H2O CO32-+H3O+ CO32-+H3O+ |
| D.次氯酸的结构式:H-Cl-O |
有两种饱和一元醇的混合物4.0g,与4.6g钠反应,生成 的H2在标准状况下的体积为1120ml,这两种醇分子中相差一个碳原子,则这两种醇为
| A.甲醇、乙醇 | B.乙醇、1-丙醇 |
| C.乙醇、2-丁醇 | D.无法判断 |
对下图两种化合物的结构或性质描述正确的是
| A.不是同分异构体 |
| B.分子中共平面的碳原子数相同 |
| C.均能与溴水反应 |
| D.可用红外光谱区分,但不能用核磁共振氢谱区分 |
下列化合物中同分异构体数目最少的是
| A.C5H12 | B.C5H11OH | C.C5H10 | D.C4H8O2 |
图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法错误的是
| A.分子中含有三种含氧官能团 |
| B.1 mol 该化合物与NaOH(aq) 反应,最多消耗量4 mol NaOH |
| C.既可以发生取代反应,又能够发生加成反应 |
| D.既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2 |
某有机物的结构简式如图,关于该物质的叙述错误的是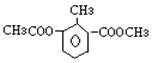
| A.一个分子中含有12个H原子 |
| B.一氯代物有5种 |
| C.能使酸性KMnO4溶液褪色 |
| D.1mol该物质分别与足量H2、NaOH溶液反应,消耗H2、NaOH的物质的量均为3mol |