某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用托盘天平称量25.20gNaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
下列推断正确的是
| A.SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 |
| B.Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同 |
| C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少最紫色石蕊试液,充分振荡后溶液呈红色 |
下列说法中不正确的是
| A.液氨、液态氯化氢都是电解质 |
| B.Na2O2、HClO、SO2等物质都具有漂白作用 |
| C.置换反应都是氧化还原反应,复分解反应都是非氧化还原反应 |
| D.明矾能水解生成氢氧化铝胶体,可用作净水剂 |
已知某可逆反应:2M(g) N(g) △H<0。现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示。下列说法中,正确的是
N(g) △H<0。现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示。下列说法中,正确的是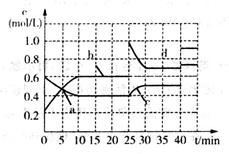
| A.a、b、c、d四个点中处于平衡状态的点是a、b |
| B.反应进行至25 min时,曲线发生变化的原因是加入了0.4 mol N |
| C.若调节温度使35 min时体系内N的体积分数与15 min时相等,应升高温度 |
| D.若在40 min时出现如图所示变化,则可能是因为加入催化剂引起的 |
下列说法中,正确的是
| A.常温下,某NaHSO3溶液的pH<7,则该溶液中c(SO32-)<c(H2SO3) |
| B.25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,所消耗溶液体积为:V(醋酸溶液)>V(NaOH溶液) |
| C.将l mL pH=2的醋酸溶液加水稀释到10 mL,pH变为3 |
D.常温下,将Na2CO3溶液加水稀释,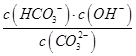 的值增大 的值增大 |
实验室需配制一种溶液,除水电离出的离子外还含有五种离子,且在该溶液中这五种离子的物质的量浓度均为l mol·L-1,下面四个选项中,能达到此要求的是
| A.Al3+、K+、SO42-、Cl-、HCO3- | B.Fe2+、H+、Br-、NO3—、Cl- |
| C.Na+、K+、SO42-、NO3—、Cl- | D.Al3+、Na+、Cl-、SO42-、NO3— |