下列事实一定能证明HNO2是弱电解质的是
①常温下HNO2溶液的pH小于7 ②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应 ④0.1 mol/L HNO2溶液的pH=2.1
⑤NaNO2和H3PO4反应,生成HNO2 ⑥pH=1的HNO2溶液稀释至100倍,pH约为2.8
⑦常温下NaNO2溶液的pH大于7
| A.①④⑥ | B.①②③④ | C.④⑤⑥⑦ | D.全部 |
在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是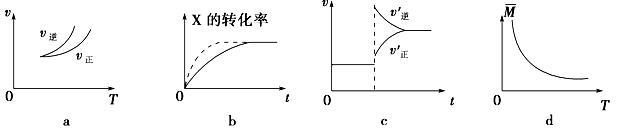
| A.依据图a可判断正反应为吸热反应 |
| B.在图b中,虚线可表示压强增大 |
| C.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
在密闭容器中进行反应X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
| A.Z为0.2 mol·L-1 | B.Y2为0.35 mol·L-1 |
| C.X2为0.3 mol·L-1 | D.Z为0.4 mol·L-1 |
某恒容密闭容器中发生可逆反应:A(s)+B(g) C(g),能说明该反应已达到平衡状态的是
C(g),能说明该反应已达到平衡状态的是
A.容器内A、B、C三者共存
B.v(C)=v(B)
C.容器内压强不再变化
D.气体的密度不再变化
下图曲线a表示反应X(g)+Y(g) +N(s)  Z(g)+M(g) △H<0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g) △H<0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
| A.升高温度 |
| B.加大N的投入量 |
| C.缩小体积 |
| D.加大X的投入量 |
下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 |
| B.用铁粉代替铁钉与稀硫酸反应制取氢气 |
| C.合成氨工业中使用催化剂 |
| D.在试管中进行铝和盐酸反应时,稍微加热 |