在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是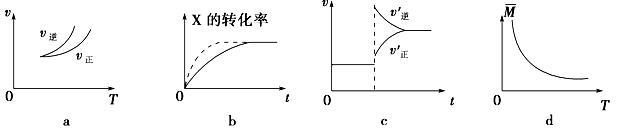
| A.依据图a可判断正反应为吸热反应 |
| B.在图b中,虚线可表示压强增大 |
| C.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
读世界某区域图,回答各题。
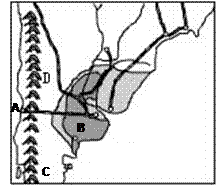
关于图中山脉D的形成,叙述正确的是
| A.非洲板块与印度洋板块相撞形成 |
| B.太平洋板块与美洲板块相撞形成 |
| C.南极洲板块与美洲板块相撞形成 |
| D.太平洋板块与大西洋板块相撞形成 |
关于图中C处的自然带的叙述正确的是
| A.温带落叶阔叶林带,属于经度地带性分布 |
| B.温带落叶阔叶林带,属于垂直地带性分布 |
| C.亚热带常绿硬叶林带,属于纬度地带性分布 |
| D.温带荒漠带,属于非地带性分布 |
下列四图中,正确表示A处气候资料的是
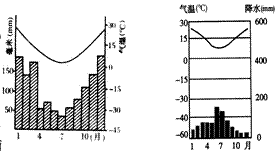 |
|||||
 |
|||||
 |
|||||
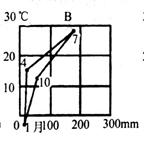
27、关于图中B处的农业农业地域类型,正确的叙述是()
| A.混合农业、专业化程度很高 |
| B.大牧场放牧业,对国际市场依赖性大 |
| C.商品谷物农业,经营的规模很大 |
| D.季风水田农业,水力工程量大 |
读图,图中等值线为地球自转线速度等值线,完成各题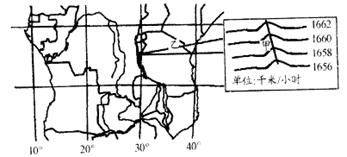
根据图中等值线分析,造成甲处等值线弯曲的原因是
| A.山岭 | B.峡谷 | C.温度 | D.洋流 |
甲地地形区的成因是
| A.流水侵蚀而形成的 |
| B.两大板块张裂而形成的 |
| C.岩层断裂陷落而形成的 |
| D.地下岩浆上升冷却而形成的 |
关于乙地区的气候类型和成因,都正确的是
| A.热带草原气候,地势高 |
| B.热带雨林气候,赤道低气压带控制 |
| C.地中海气候,西风带和副热带高气压带交替控制 |
| D.热带沙漠气候,副热带高气压带控制 |
读世界四地的关联图。回答各题。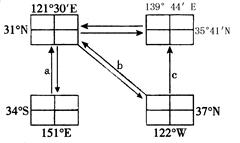
如果图中箭头abc表示四地所在国家之间国际贸易中的某种农产品,则该农产品是
| A.玉米 | B.小麦 |
| C.稻米 | D.大豆 |
如果图中箭头b表示电子工业的区位转移,则迁入地的区位优势主要是
①地价因素②技术因素③劳动力因素④资金因素
| A.①② | B.②③ | C.①③ | D.②④ |
读我国两个三角洲略图,回答各题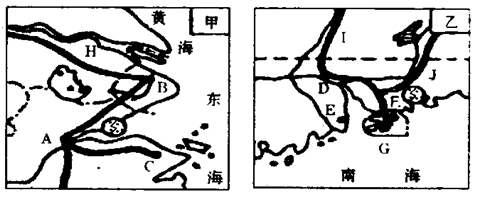
下列工业基地与其所在三角洲的组合中,正确的是
| A.京津唐工业基地——甲三角洲 | B.沪宁杭工业基地——乙三角洲 |
| C.珠江三角洲工业基地——乙三角洲 | D.辽中南重工业基地——甲三角洲 |
20世纪90年代以来,为了缓解甲、乙三角洲地区的能源供应紧张问题,两地都很重视开发和利用的新能源是
| A.水能 | B.太阳能 | C.核能 | D.天然气 |
读我国某省区图。完成各题。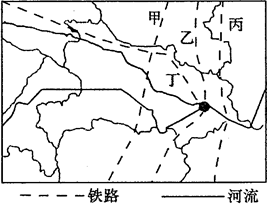
图中铁路线直达广州的是
| A.甲 | B.乙 | C.丙 | D.丁 |
该省省会城市形成和发展的最主要的自然条件是
| A.气候湿润 | B.地形平坦 | C.土壤肥沃 | D.河流交汇 |
下列我国重大工程位于或通过该省区的有
①南水北调②西电东送③西气东输④三峡工程
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |