(16分)根据题目要求作答:
(1)下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,正确的是 。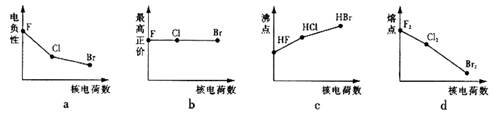
(2)下列物质变化,只与范德华力有关的是 。
A.干冰熔化
B.冰的汽化
C.乙醇与水混溶
D.碘溶于四氯化碳
E.石英熔融
(3)已知0.1 mol CrCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.2 mol AgCl沉淀。此配合物最有可能的化学式是 。
A.[Cr(H2O)6]Cl3 B.[Cr(H2O)5Cl]Cl2·H2O
C.[Cr(H2O)4Cl2]Cl·2H2O D.[Cr(H2O)3Cl3]·3H2O
(4)金属镍在电池、合金、催化剂等方面应用广泛。Ni是元素周期表中第28号元素。
①第2周期基态原子未成对电子数与Ni相同且电负性最小的元素是 ;
②NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
③CO与N2结构相似,CO分子内σ键与π键个数之比为 。Ni、Fe、Co等金属都能与CO反应形成配合物 ,Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属
于 (填晶体类型 )。
④普鲁士蓝是一种配合物,可用作染料,它的晶胞结构如图所示(其中K+在体心位置,未标出),普鲁士蓝中 n(Fe3+)∶n(CN一)= _____ 。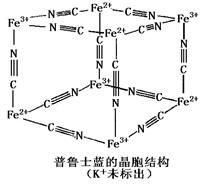
下表列出了A~G7种元素在周期表中的位置:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
C |
D |
E |
|||||
| 3 |
B |
F |
G |
|||||
| 4 |
A |
(1)分别写出A、D、G的元素符号:、、,其中化学性质最不活泼的是(填元素符号);
(2)F的氢化物中化学键的类型是,F的最高价氧化物对应的水化物的化学式是;
(3)C、D、E三种元素中,氢化物种类最多的是;
(4)写出B与F形成的化合物发生水解反应的离子方程式;
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)写出下列溶液中溶质的化学式
A___________,C_______________,E______________,F_________________。
(2)E的浓溶液与Cu应的化学方程式是______________________________________________________;该反应中氧化剂与还原剂的物质的量之比为____________;该反应的还原产物与少量B溶液反应的离子方程式是_____________________________________________________________________________。
(3)如何通过实验进一步确定D溶液的溶质?写出简要的操作及现象_____________________________。
X2、Y2单质在一定条件下有如下反应:X2+Y2+H2O→HXO3+HY(未配平)。
按要求回答下列问题:
(1)X2、Y2可能的组合是__________________。
a.F2、Br2 b.I2、Cl2c.C12、O2 d.Br2、N2
(2)试比较X2、Y2、HXO3的氧化性强弱:___________________[用(1)中所选的X2、Y2回答,下同]。判断HXO3+HX能否反应:___________(填“能”或“不能”)。若能反应,请写出其化学反应方程式,若不能反应,请说明理由:____________________。
(3)若用KX制取HX,不能选用浓硫酸的原因是________________________。(用化学方程式表示)
(4)工业上测定某产品中YO-的含量,先将一定量产品的溶液加入过量的KX溶液和稀硫酸中,使之反应生成X2,试写出上述反应的离子方程式:______________________。
(5)Fe2+、Fe3+、X2、X-、Y-五种微粒中的两种微粒A(阳离子)和B在溶液中能相互反应生成X2,向含微粒A的溶液中滴入足量l mol/LNa2S溶液,生成的沉淀C与足量的热NaOH溶液反应,过滤,残渣D再与稀硫酸完全反应生成E溶液。则生成的沉淀C的成份是(填化学式)____________________。E溶液中阳离子除H+外,另外的阳离子的检验方法是_______________________________________。
银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下图: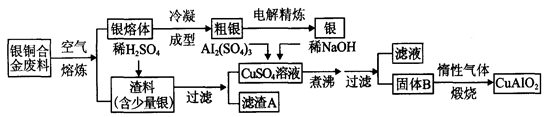
(1)电解精练银时,阴极反应式为_______________;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该红棕色气体与水反应的化学方程式为_______________________________________。
(2)固体混合物B的组成为_____________;在生成固体B的过程中,必须控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为_____________________。
(3)煅烧过程中生成的氧化产物与NH3在催化剂条件下反应的化学方程式为_____________________。这个反应中会有白烟产生,该白烟为______________。
(4)若银铜合金中铜的质量分数为64%,理论上3.0kg废料中的铜可完全转化为__________molCuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液___________L。
下列实验流程图中,X为第三周期两种重要单质的氧化物的混合物。反应②、④是工业上的重要反应,部分物质及反应条件没有列出。
请回答下列问题:
(1)写出A、E、B的化学式:A________, E___________,B___________。
(2)写出C溶液转化为C固体的过程中,HCl气流的作用:________________________。
(3)写出①、③、④反应的化学方程式,(若是离子反应写离子方程式)
①__________________________________________________;
③__________________________________________________;
④__________________________________________________。
(4)将SO2气体分别通入下列溶液写出对应的实验现象
①BaCl2溶液________________________________;
②Ba(NO3)2溶液_____________________________________;
⑨FeCl3溶液_____________________________。