下列说法错误的是
| A.钠在空气中燃烧最后所得产物为Na2O2 |
| B.镁因在空气中形成了一薄层致密的氧化膜,保护了里面的镁,故镁不需要像钠似的进行特殊保护 |
| C.铝制品在生活中非常普遍,这是因为铝不活泼 |
| D.铁在潮湿的空气中因生成的氧化物很疏松,不能保护内层金属,故铁制品往往需涂保护层 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是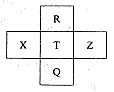
| A.X元素的最高价氧化物对应的水化物酸性强于T元素 |
| B.原子半径:R<T<Z |
| C.Z的单质可从T的气态氢化物中置换出T的单质 |
| D.R、T、Q最高正价相同 |
化学已渗透到人类生活的各个方面,下列说法中不正确的是
| A.BaSO4和BaCO3均难溶于水,均可用作“钡餐” |
| B.轮船的外壳和铁锅等生锈主要发生了电化学腐蚀 |
| C.钻石和水晶都是人们熟知的宝石,但其化学成分不同 |
| D.硫酸铁和明矾都可用于净水 |
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)= 0.04 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于0.5
25 ℃时,用0.100 0 mol·L-1 NaOH溶液滴定20 mL 0.100 0 mol·L-1一元酸HA(pKa="-lg" Ka=4.75)溶液,其滴定曲线如图所示,下列说法正确的是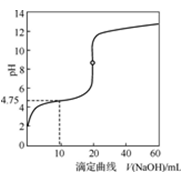
A.当滴定到pH=4.75时,c(Na+)>c(A-)=c(HA)>c(OH-)
B.当溶液中c(H+)+c(OH-)=2×10-7时: c(Na+)=c(A-)>c(OH-)=c(H+)
C.当滴入NaOH溶液20 mL时,c(OH-)=c(H+)+c(HA)
D.当滴入40 mL NaOH溶液时,溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 |
X产生氢气的体积比Y多 |
金属性:X>Y |
| B |
等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 |
HA放出的氢气多且反应速率快 |
HA酸性比HB强 |
| C |
将浓硫酸滴到蔗糖表面 |
固体变黑色膨胀 |
浓硫酸有脱水性和强氧化性 |
| D |
将FeSO4高温强热,得红色固体,产生的气体全部通入足量BaCl2溶液 |
产生白色沉淀 |
白色沉淀为BaSO4和BaSO3 |