(Ⅰ)水的电离平衡曲线如下图所示。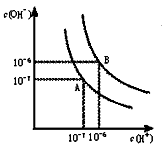
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将100℃下的pH=8的Ba(OH)2溶液与100℃下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。 (Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
(3)若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
(4)若上述关系中C是正确的,则溶液中溶质的化学式是 。
(5)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系是c(NH4+) c(Cl-)。
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。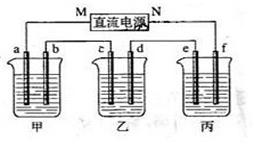
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;
极;
②电极b上发生的电极反应为;
③计算电极b上生成的气体在标准状态下的体积:;
④电极c的质量变化是g;
⑤电解前后各溶液的PH大小是否发生变化(填变大、变小、不变):
甲溶液;乙溶液 ;丙溶液
;丙溶液
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大.A的原子核无中子,能与B、C分别形成10电子的化合物;B、C 的质子数之和与E的质子数相等,B、C的族序数为奇数;D、E位于同一周期,D的阳离子所带的正电荷数等于该阳离子的电子层数.试回答下列问题:
的质子数之和与E的质子数相等,B、C的族序数为奇数;D、E位于同一周期,D的阳离子所带的正电荷数等于该阳离子的电子层数.试回答下列问题:
(1)C与D形成的化合物的电子式.
(2)写出D的单质与CO2反应的化学方程式.
(3)“嫦娥 一号”发射所用的液体燃料是上述(填元素名称)元素的单质.
一号”发射所用的液体燃料是上述(填元素名称)元素的单质.
(4)工业上,使元素E的低价氧化物转化为其最高价氧化物的设备名称为.
(5)在一定的条件下,A2、B2混合物经过一段时间的反应后,B2的浓度减小了0. 3 mol/L.[此时间内A2表示的化学反应速率为0. 45 mol/(L·s).则此段反应时间为s
(6分)已知在25℃,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,
Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17。
(1)判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量/1 L溶液表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为____________________________。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)________(填“增大”“减小”或“不变”)。
(3)在25℃时,若取0.188 g的AgY(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为__________________。
(4)由上述Ksp判断,在上述(3)的体系中,________(填“能”或“否”)实现AgY向AgZ的转化,简述理由:________________________________________。
(1)实验室可用无水乙醇处理少量残留的金属钠,化学反应方程式为_______________。要清洗附着在试管壁上的硫,可用的试剂是________。
(2)如图所示为钠硫高能电池的结构示意图。该电池的工作温度为320℃左右,电池反应为2Na+xS=Na2Sx,负极的电极反应式为________,正极的电极反应式为________。M(由Na2O和Al2O3制得)的两个作用是________________。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的________倍。(Pb的相对原子质量为 207)
(3)Na2S溶液水解的化学方程式。溶液中离子浓度由大到小的顺序为_______,向该溶液中加入少量固体CuSO4,溶液pH________(填“增大”“减小”或“不变”)。