下列有关物质的性质或应用说法正确的是
| A.氢氧化钠用于治疗胃溃疡病人的胃酸过多症 |
| B.金属钠具有强的还原性,可利用钠和TiCl4溶液反应制取金属Ti |
| C.糖类、油脂、蛋白质在一定条件下均可以水解 |
| D.在常温下,浓硫酸、浓硝酸能用铁罐储运 |
下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol |
| D.己知2C(s)+2O2(g)=2CO2(g);△H12C(s)+O2(g)=2CO(g);△H2则△H1>△H2 |
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是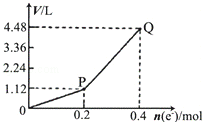
| A.电解过程中,溶液的pH不断增大 |
| B.Q点对应的气体中,H2与O2的体积比为2:1 |
| C.阳极电极反应式为2H2O+4e﹣=4H++O2↑ |
| D.当转移0.4mol e﹣时,电解生成的铜为6.4g |
反应4NH3(气)+5O2(气)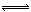 4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率 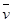 (X)(反应物的消耗速率或产物的生成速率)可表示为
(X)(反应物的消耗速率或产物的生成速率)可表示为
A.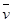 (NH3) =" 0.010" mol/(L·s) (NH3) =" 0.010" mol/(L·s) |
B.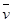 (O2) =" 0.0010" mol/(L·s) (O2) =" 0.0010" mol/(L·s) |
C.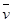 (NO) =" 0.0010" mol/(L·s) (NO) =" 0.0010" mol/(L·s) |
D.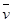 (H2O) =" 0.045" mol/(L·s) (H2O) =" 0.045" mol/(L·s) |
反应A+B C(ΔH>0)分两步进行:① A+B
C(ΔH>0)分两步进行:① A+B X(ΔH<0),② X
X(ΔH<0),② X C(ΔH>0)。下列示意图中,能正确表示总反应过程中能量变化的是
C(ΔH>0)。下列示意图中,能正确表示总反应过程中能量变化的是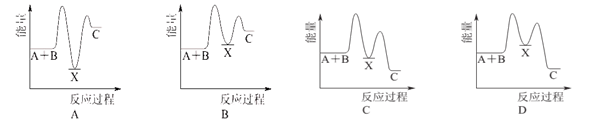
有甲、乙两个装置,下列说法错误的是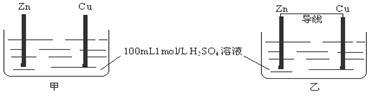
| A.甲、乙装置中,Zn的质量均减小 | B.甲、乙装置中,Cu上均有气泡产生 |
| C.化学反应速率 乙 > 甲 | D.甲中H+ 移向Zn,乙中H+ 移向Cu |