工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g)+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
(1)从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2) =____ ;平衡时CO的转化率为____ 。
(2)该反应的平衡常数表达式为 ;若升高反应温度,该反应的平衡常数将 (填“增大”、“减小”或“不变”)。
(3)若在一定温度下,向一恒压容器中充人1 mol CO、2mol H2和1 mol CH3OH,反应达到平衡时,测得混合气体的密度是同温同压下起始混合气体密度的0.8倍,则到达平衡状态前该反应向____ (填“正”或“逆”)反应方向进行。
(4)根据图二,甲醇分解的热化学方程式为 。
(5)若以甲醇为原料制成燃料电池,在碱性介质中负极的电极反应式为____ 。
A、B、C、D、E、F、G为常见物质,其中C为淡黄色固体。甲、乙、丙为常见气体。各物质的转化关系如下图所示。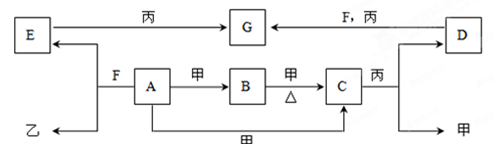
回答下列问题:
(1)C的名称是;D的俗称__________;F的化学式;
A+甲→C的反应条件是。
(2)在一定条件下,甲+乙→F,该反应属于。
①氧化还原反应②非氧化还原反应③化合反应④分解反应
⑤复分解反应 ⑥置换反应⑦离子反应
(3)写出下列变化的离子方程式。
①A+F→E+乙:
 。
。
②D+F+丙→G:。
(1)已知2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是,氧化产物是。若生成氯气11.2L(标准状况),则转移电子的物质的量为mol。
(2)配置0.2mol/L的NaCl溶液450mL, 需要用到的仪器有托盘天平(含砝码)、药匙、烧杯、玻璃棒、_____________和______,需要用托盘天平称取NaCl__________g。
(3)漂白粉的有效成分是_______________
(4)已知每1 克氢气完全燃烧生成水蒸气时将放出121kJ热量,写出该反应的热化学方程式___________________________________________
25℃时,0.1mol·L-1 HA溶液pH=2,0.1mol·L-1 HB溶液pH=3。
(1)前 者大于后者的是(多选、错选均不给分,下同);
者大于后者的是(多选、错选均不给分,下同);
①HA、HB的电离平衡常数②HA、HB的电离度③溶液中的c(OH-)
④溶液的导电性⑤溶液中由水电离出的c(H+)
(2)若HA、HB溶液的pH相同、体积相等,前者小于后者的是;
①HA、HB物质的量浓度 ②同时加入足量的锌,开始反应时速率
③同时加入足量的锌,反应完全后生成H2的质量 ④二种酸溶液的导电能力
⑤用1mol/LNaOH溶液分别中和二种酸,消耗NaOH溶液体积
⑥将这两种溶液分别稀释10倍后溶液的pH。(3)若中和体积为Va浓度为0.1mol·L-1 HA溶液,消耗0.1mol·L-1 NaOH溶液的体积为Vb,且Va>Vb,下列说法一定正确的是。(提示:CH3COONa溶液呈碱性)
①混合后溶液呈中性②混合后溶液呈酸性 ③混合后溶液呈碱性
③混合后溶液呈碱性
④混合后溶液中的溶质为NaA⑤混合后溶液中的溶质为NaA和HA
⑥混合后溶液中的溶质为NaA和NaOH
在容积为VL的密闭容器中发生2NO2 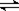 2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
(1)若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是。
A.有、无催化剂 B.温度不同 C.压强不同 D.V值不同
(2)写出该反应的化学平衡常数K的表达式:,
并比较K800℃K850℃(填“>”、“<”或“=”)。
(3)在图上作出在A条件下NO的变化曲线,并求算在B条件下从反应开始至达到平衡,氧气的反应速率v(O2)=。
(4)不能说明该反应已达到平衡状态的是。
A.v正(NO2)=v逆(NO)B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变 D.气体的密度保持不变
(5)在如图所示的三个容积相同的三个容器①、②、③进行反应:2NO+O2  2NO2
2NO2
若起始温度相同,分别向三个容器中充入2molNO和1molO2 ,则达到平衡时各容器中NO物质的百分含量由大到小的顺序为(填容器编号)。
如右图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为极,A极的电极反应式为。若所盛溶液为KCl溶液:则B极的电极反应式为, K+移向极(填A、B)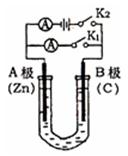
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是。
②B电极上的电极反应式为,总反应化学方程式是 。
。
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的。
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是,电极反应式是,反应一段时间后电解质溶液中Cu2+浓度(填“增大”、“减小”、“不变”)。